
有两种晶体A和B,它们分别为白色和无色,把A加热可得到盐C和气体D,把B在一定条件下加热可得盐E和气体F.让单质G在足量的F中燃烧,可得淡黄色固体H,让D通过H又可得C和F.把E和浓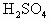 共热,可得气体I,把I通入C的溶液也可得D.把I的浓溶液滴入B中,可得一种黄绿色气体J.B的焰色反应是浅紫色(透过蓝色钴玻璃片).
共热,可得气体I,把I通入C的溶液也可得D.把I的浓溶液滴入B中,可得一种黄绿色气体J.B的焰色反应是浅紫色(透过蓝色钴玻璃片).
由此推断:A为________,B为________,C为________,D为________,E为________,F为________,G为________,H为________,I为________,J为________.
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
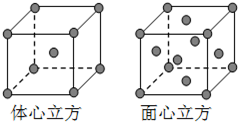 Fe为过渡元素,它的原子序数为26.回答下列问题:
Fe为过渡元素,它的原子序数为26.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
31 |
30 |
| 2 |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 (1)图表法、图象法是常用的科学研究方法.短周期某主族元素M的电离能情况如图(A)所示.则M元素位于周期表的第
(1)图表法、图象法是常用的科学研究方法.短周期某主族元素M的电离能情况如图(A)所示.则M元素位于周期表的第| 2 | 3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com