
| A. | H2和D2互为同位素 | B. | 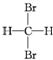 和 和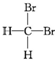 互为同分异构体 互为同分异构体 | ||
| C. | 戊烷有两种同分异构体 | D. | 金刚石与石墨是同素异形体 |
分析 A.质子数相同,中子数不同的同种元素的不同原子互称为同位素;
B.依据甲烷结构是正四面体结构分析,碳原子形成四个共价键形成的空间结构为四面体结构;
C.烷烃同分异构体书写:先写最长链;然后从最长链减少一个碳原子作为取代基,在剩余的碳链上连接,即主链由长到短,支链由整到散,位置由中心排向两边.注意从母链取下的碳原子数,不得多于母链所剩余的碳原子数;
D.同种元素组成的不同单质为同素异形体.
解答 解:A.质子数相同,中子数不同的同种元素的不同原子互称为同位素,H2和D2不是原子是分子,不是同位素,故A错误;
B.甲烷结构是正四面体结构,碳原子形成四个共价键形成的空间结构为四面体结构, 和
和 是同种物质,不是同分异构体,故B错误;
是同种物质,不是同分异构体,故B错误;
C.戊烷存在正戊烷、异戊烷和新戊烷三种同分异构体,CH3CH2CH2CH2CH3、 、
、
所以戊烷有3种同分异构体. 故C错误;
D.同种元素组成的不同单质为同素异形体,金刚石与石墨是碳元素的不同单质,是碳元素的同素异形体,故D正确;
故选D.
点评 本题考查了同分异构体、同位素、同素异形体的概念、饱和烷烃分子结构等知识点,难度不大,注意把握概念的内涵与外延.


科目:高中化学 来源: 题型:选择题
| A. | 某单核粒子的核外电子排布为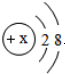 ,则该微粒一定是氖原子 ,则该微粒一定是氖原子 | |
| B. | 原子最外层只有1个电子的元素一定是金属元素 | |
| C. | NH4+与H3O+具有相同的质子数和电子数 | |
| D. | 最外层电子数是次外层电子数2倍的原子容易失去电子成为阳离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
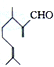 )是一种重要的香料,在硫酸的作用下能生成对异丙基甲苯(
)是一种重要的香料,在硫酸的作用下能生成对异丙基甲苯(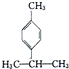 ).下列有关香叶醛与对异丙基甲苯的叙述正确的是( )
).下列有关香叶醛与对异丙基甲苯的叙述正确的是( )| A. | 对异丙基甲苯的分子式为C10H14 | |
| B. | 香叶醛的一种同分异构体可能是芳香醇 | |
| C. | 两者互为同分异构体 | |
| D. | 两者均能与溴水反应加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
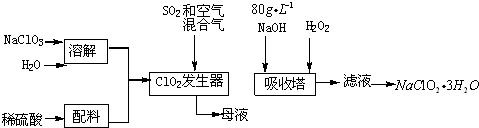
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a c f h | B. | a c e g | C. | a c e f h | D. | b d e h |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
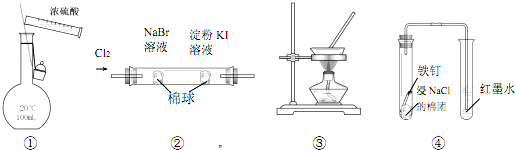
| A. | 图①装置可用于配制 100 mL 0.1 mol/L的硫酸 | |
| B. | 图②装置可证明氧化性:Cl2>Br2>I2 | |
| C. | 图③装置可通过蒸干AlCl3饱和溶液制备AlCl3晶体 | |
| D. | 图④装置可观察铁的吸氧腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | pH=3的醋酸与pH=11的氢氧化钠溶液等体积混合所得溶液的pH<7 | |
| B. | 反应2CO(g)+2H2(g)→CH3COOH (l)的△S>0 | |
| C. | 冰醋酸用水稀释,溶液中c(H+)先变大后变小 | |
| D. | 含有CH3COOH、C2H5OH、CH3COOC2H5及H2O的平衡体系中加入少量浓硫酸,CH3COOC2H5的物质的量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
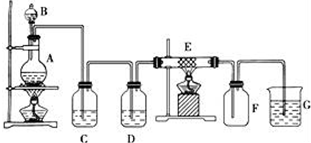
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气:K+ Ba2+ SiO32- NO3- | |
| B. | 氨气:K+ Na+ AlO2- CO32- | |
| C. | 二氧化硫:Na+ NH4+ SO32- C1- | |
| D. | 甲醛:Ca2+ Mg2+ Mn04- NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com