
| A. | 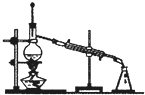 石油蒸馏 | B. |  检验Fe3+ | C. |  制备氨气 | D. |  中和滴定 |
分析 A.蒸馏测定馏分的温度,冷水下进上出;
B.铁离子与KSCN溶液结合生成络离子,溶液为血红色;
C.浓氨水与CaO混合,为固体与液体制取氨气的原理;
D.图中为酸式滴定管,不能盛放碱性溶液.
解答 解:A.蒸馏测定馏分的温度,冷水下进上出,则图中蒸馏装置合理,故A正确;
B.铁离子与KSCN溶液结合生成络离子,溶液为血红色,则图中检验铁离子的实验装置合理,故B正确;
C.浓氨水与CaO混合,为固体与液体制取氨气的原理,CaO与水反应放热且氢氧根离子浓度增大,使NH3+H2O?NH3•H2O?NH4++OH-平衡逆向移动,氨气逸出,故C正确;
D.图中为酸式滴定管,不能盛放碱性溶液,应利用碱式滴定管盛放NaOH溶液,故D错误;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及混合物分离提纯实验装置、离子检验、气体制备、中和滴定等,把握物质的性质、反应原理、实验装置的作用等为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ②③④ | B. | ③④ | C. | ①②③ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室.分别向A、B两室充入H2、O2的混合气体和1mo1空气.此时活塞的位置如图所示.
室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室.分别向A、B两室充入H2、O2的混合气体和1mo1空气.此时活塞的位置如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素 | X | Y | Z | W |
| 原子半径/pm | 186 | 143 | 75 | 71 |
| 主要化合价 | +1 | +3 | +5、+3、-3 | -1 |
| A. | X、Y元素的金属性X<Y | |
| B. | Z的气态氢化物比W的气态氢化物稳定 | |
| C. | Y的最高价氧化物对应的水化物能溶于稀氨水 | |
| D. | 四种元素对应的简单离子的离子半径大小顺序为Z3->W->X+>Y3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 基态原子的4S能级中只有1个电子的元素共有4种 | |
| B. | ${\;}_{17}^{35}$Cl与${\;}_{17}^{37}$Cl得电子能力不相同 | |
| C. | Cl-、S2-、Na+、K+半径逐渐减小 | |
| D. | 最外层有3个未成对电子的原子一定属于主族元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 离子 | Fe3+ | Al3+ | ZrO2+ |
| 开始沉淀时pH | 1.9 | 3.3 | 6.2 |
| 完全沉淀时pH | 3.2 | 5.2 | 8.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 可逆反应2A+B?2C(g)△H<O,在一密闭容器中进行,随T(℃)变化容器中气体平均相对分子质量$\overline{M}$r的变化如图所示,则下列叙述中正确的是( )
可逆反应2A+B?2C(g)△H<O,在一密闭容器中进行,随T(℃)变化容器中气体平均相对分子质量$\overline{M}$r的变化如图所示,则下列叙述中正确的是( )| A. | A和B可能都是固体 | |
| B. | A和B一定都是气体 | |
| C. | A和B可能都是气体 | |
| D. | 随温度的升高,容器中的压强一定在减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com