
��.��һ�������£���1.00molN2(g)��3.00molH2(g)�����һ��10.0L�ܱ������У��ڲ�ͬ�¶��´ﵽƽ��ʱNH3(g)��ƽ��Ũ����ͼ��ʾ�������¶�ΪT1ʱƽ���������а������������Ϊ25.0%��
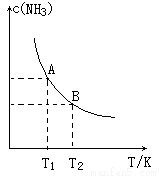
(1)���¶���T1�仯��T2ʱ��ƽ�ⳣ����ϵK1___________K2(���������������=��)���ʱ��H___________0��(���������)
(2)�÷�Ӧ��T1�¶���5.0min�ﵽƽ�⣬���ʱ����N2�Ļ�ѧ��Ӧ����Ϊ___________,N2��ת����___________��
(3)T1�¶��¸÷�Ӧ�Ļ�ѧƽ�ⳣ��K1=___________��
(4)T1�¶�ʱ������ø�¯��c(N2)=0.5mol/L��c(H2)=0.5mol/L��c(NH3)=0.5mol/L����������£��÷�Ӧ�Ƿ���ƽ��״̬___________(���ǻ��)����ʱ��Ӧ������v��___________v��(�������=)��
��.�������� �о��������ڳ��³�ѹ����������N2�ڴ���������ˮ������Ӧ��2N2(g)+6H2O(l)��4NH3(g)+3O2(g)��
�о��������ڳ��³�ѹ����������N2�ڴ���������ˮ������Ӧ��2N2(g)+6H2O(l)��4NH3(g)+3O2(g)��
(1)�˷�Ӧ�ġ�S 0(���������)��
��֪2CO(g)+2NO(g)=N2(g)+2CO2(g) ��H=-a kJ��mol-1
2NO(g)+O2(g)=2NO2(g) ��H =-b kJ��mol-1��CO��ȼ���ȡ�H =-c kJ��mol-1��
(2)д����������β����NO2����Ⱦʱ��NO2��CO�ķ�Ӧ���Ȼ�ѧ��Ӧ����ʽ

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���Ĵ�ʡ��һ�����л�ѧ���������棩 ���ͣ�ѡ����
���������������ļӿ죬�����С��װʳƷ�ѱ��㷺���ܣ�Ϊ�˷�ֹ��ʳƷ�������ʣ��ӳ�ʳƷ�ı����ڣ��ڰ�װ���г����뿹�������ʡ����в����ڿ��������ʵ���
A����ʯ�� B����������(Na2SO3) C������ D����������(FeSO4)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ĸ�һ���¿�����ѧ���������棩 ���ͣ�ѡ����
��m g��������������ͭ��������������ƷͶ�����ʵ���Ũ��Ϊ1 mol/L��2 L������ǡ����ȫ��Ӧ������������ĸ���Ʒ��ͨ�����������������ȣ���ַ�Ӧ�����ý�����������( )
A��(m��16)g B��(m +16)g C��(m��32 )g D��16g
+16)g C��(m��32 )g D��16g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ĸ�һ���¿�����ѧ���������棩 ���ͣ�ѡ����
���� ������������ɫ��Һ���ܴ���������� ( )
������������ɫ��Һ���ܴ���������� ( )
A��Na+��Ba2+��Cl?��SO42-
B��Ca2+��HCO3?��OH?��K+
C��MnO4?��K+��I?��H+
D��OH?��Cl?��Na+��CO32?
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ĸ�һ���¿�����ѧ���������棩 ���ͣ�ѡ����
���л�ѧ��Ӧ����������ԭ��Ӧ��ˮ�Ȳ����������ֲ�����ԭ������( )
A��CaO+H2O=Ca(OH)2
B��NaH+H2O=NaOH+H2��
C��3NO2+H2O=2HNO3+NO
D��2H2O+2F2=4HF+O2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ĸ߶����¿�����ѧ���������棩 ���ͣ�ѡ����
��AgCl�ֱ����ʢ�У���5 mLˮ����6 mL0.5mol/L NaCl��Һ����10 mL 0.2 mol/LCaCl2��Һ����50 mL0.1mol/L������ձ��У����й���ʣ�࣬����Һ��c(Ag+)�Ӵ�С��˳��������ȷ���� ( )
A. �ܢۢڢ� B. �ڢۢܢ� C. �٢ܢۢ� D. �٢ۢڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ĸ߶����¿�����ѧ���������棩 ���ͣ�ѡ����
���ʵ���Ũ����ͬ�������� NaX��NaY��NaZ����Һ�������ǵ�pHֵ����Ϊ8��9��10����HX��HY��HZ��������ǿ����������˳���� ( )
A��HX��HZ��HY B��HZ��HY��HX C��HX��HY��HZ D��HY��HZ��HX
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ĸ߶����¿�����ѧ���������棩 ���ͣ�ѡ����
�����Ȼ�ѧ����ʽS(l)+O2(g)�TSO2(g)��H=��293.23kJ��mol��1����������˵������ȷ����( )
A��1mol����S����ȼ�շų�����������293.23 kJ
B��1mol����S����ȼ�շų�������С��293.23 kJ
C��1 mol SO2(g)�ļ��ܵ��ܺʹ���1 mol S(l)��1 mol O2(g)�ļ���֮��
D��1 mol SO2(g)�ļ��ܵ��ܺ�С��1 mol S(l)��1 mol O2(g)�ļ���֮��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ�������¿�����ѧ���������棩 ���ͣ������
�о������к�����ͺ�̼�������ת���Ի�������������Ҫ���塣
(1)SO2�Ĵ����ŷŻ��������صĻ��������� ����ʪ�����£�д��������SO2ת��ΪHSO3-�ķ���ʽ ��
(2)�����е�����ɽ�������H2S��������Ӧ������SO42-��������Ӧ�������仯ʾ��ͼ���£�
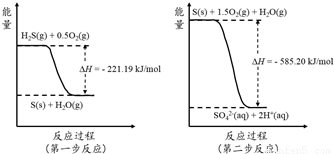
1mol H2S(g)ȫ��������SO42-(aq)���Ȼ�ѧ����ʽΪ ��
(3)SO2�ǹ�ҵ�������ԭ��֮һ��һ���¶��£����ݻ�Ϊ2L���ܱ������г���һ������SO2��O2��������Ӧ��2SO2(g)+O2(g) 2SO3(g)�������вⶨ�IJ������ݼ��±���
2SO3(g)�������вⶨ�IJ������ݼ��±���
ʱ��/min | n(SO2)/mol | n(O2)/mol |
0 | 0.10 | 0.05 |
4 | 0.04 | 0.02 |
6 | 0.02 | |
8 | 0.01 |
�ٷ�Ӧ��0-4min�ڵ�ƽ������Ϊv(SO2)= ��
�ڴ��¶��¸÷�Ӧ�Ļ�ѧƽ�ⳣ��K= ��
��8minʱ��ά���¶Ȳ��䣬��Ӧ��������ͨ��0.02mol SO2(g) ��0.01mol O2(g)�����´ﵽƽ��ʱ���������SO2�İٷֺ����� (���С�����������䡱)��
��0.01mol O2(g)�����´ﵽƽ��ʱ���������SO2�İٷֺ����� (���С�����������䡱)��
(4)��ѧ���õ����ز�����ͭ��װ����ͼ���˹����ϵͳ�����ø�װ�óɹ���ʵ������CO2��H2O�ϳ�CH4�ķ�Ӧ��
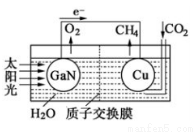
д��ͭ�缫����ĵ缫��Ӧʽ ��Ϊ��߸��˹����ϵͳ�Ĺ���Ч�ʣ�����װ���м������� (����ᡱ�����ᡱ)��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com