
| A�� | �ٺ͢ڲ�����������Ӹ�������ȣ���Ϊ1��2 | |
| B�� | �ٺ͢����ɵ����ʵ����IJ��ת�Ƶ�������ͬ | |
| C�� | ������Na������O2��Ӧ����Na2O�����¶���������Na2O�������ӿ� | |
| D�� | 25�桢101 kPa�£�Na2O2��s��+2Na��s���T2Na2O��s����H=-317 kJ/mol |
���� A��Na2O��Na2O2���������Ӹ����ȶ���1��1��
B���ֱ�����1molNa2O��Na2O2ת�Ƶ������ʵ�������2mol��
C��Na�������ڼ���ʱ���ɹ������ƣ�
D��25��ʱ�����ø�˹���ɿ�����ã�
��� �⣺A��Na2O��Na2O2���������Ӹ����ȶ���1��1�����Ԣٺ͢ڲ�����������Ӹ�������ȣ���A��ȷ��
B���ֱ�����1molNa2O��Na2O2ת�Ƶ������ʵ�������2mol�������ڢٺ͢��У�2molNa��Ӧ����1molNa2O��Na2O2��ת�Ƶ������ʵ�����ͬ����B��ȷ��
C��Na���������¶�����ʱ���ɹ������ƣ������²����������ƣ���C����
D����֪��25�桢101kPa �£�
��2Na��s��+$\frac{1}{2}$O2��g���TNa2O��s����H1=-414KJ/mol
��2Na��s��+O2��g���TNa2O2��s����H2=-511KJ/mol
�ݸ�˹���ɣ��١�2-�ڵã�Na2O2��s��+2Na��s���T2Na2O��s����H=-317kJ/mol����D��ȷ��
��ѡC��
���� ���⿼��Na�������ڱ�����������������Ӧ���ﲻͬ����������������ƽṹ������ͬʱ�����˷�Ӧ�����¶��йأ�ע���������⣮


 ����ͼ���������������ϵ�д�
����ͼ���������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
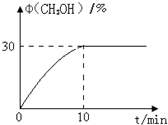 CO2����ϳɼ״��ļ������Լ������������ŷźͼ���ȼ��Σ��������Ҫ���壬��������Ҫ��Ӧ���£�CO2��g��+3H2��g���TCH3OH��g��+H2O��g�����ش��������⣺
CO2����ϳɼ״��ļ������Լ������������ŷźͼ���ȼ��Σ��������Ҫ���壬��������Ҫ��Ӧ���£�CO2��g��+3H2��g���TCH3OH��g��+H2O��g�����ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | NH4++OH-��NH3•H2O | B�� | 2Na+2H2O��2Na++2OH-+H2�� | ||
| C�� | HCO3-+OH-��H2O+CO32- | D�� | 2Na+2H2O��2NaOH+H2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1mol�κ�����������Ϊ22.4L | |
| B�� | 32g���������ԼΪ22.4L | |
| C�� | ��״���£�18gˮ�������22.4L | |
| D�� | ��״���£�1mol�κ�����������ԼΪ22.4L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C4H8 | B�� | C5H10O | C�� | CH4 | D�� | C2H4Br2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ۢ� | C�� | �ڢ� | D�� | �ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cu2+ Na + NO3- SO42- | B�� | Mg2+ Cl- Al3+ SO42- | ||
| C�� | K + Cl- HCO3- NO3- | D�� | Ca2+ Na+ Fe3+ NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NH3�����ǷǼ��Է��� | |
| B�� | ������3��N-H���ļ�������ȣ����Dz���� | |
| C�� | NH3������3��N-H���ļ�����ȣ�3�����Ƕ�����107��18�� | |
| D�� | NH3������3��N-H���ļ�����ȣ�3�����Ƕ�����120�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com