
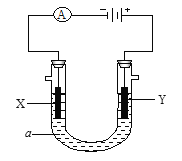
【题目】电解原理在工业中有广泛应用。如图是一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。
请回答以下问题:
(1) 若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式是: 。
在X极附近观察到的现象是: 。
②Y电极上的电极反应式是: ,
检验该电极反应产物的方法是: 。
(2) 如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是: ,电极反应式是: 。
②Y电极的材料是: ,电极反应式是: 。
(说明:杂质发生的电极反应不必写出)
【答案】(1)①2H++2e-=H2↑(2分)放出气体,溶液变红。(2分)
②2Cl--2e-=Cl2↑(2分)把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色。(2分)
(2)①纯铜(1分)Cu2++2e-=Cu(1分)
②粗铜(1分)Cu-2e-=Cu2+(1分)
【解析】
试题解析:(1) X极为电解池的阴极,发生还原反应,溶液中的氢离子得电子变氢气;2H+ + 2e- = H2↑;在阴极附近有气泡产生,溶液中氢离子浓度减小,氢氧根离子浓度增大,酚酞遇碱变红;Y电极为电解池的阳极,氯离子失电子变为氯气;2Cl- - 2e- = Cl2 ↑;氯气有氧化性,能够把碘离子氧化为碘单质,遇淀粉变蓝;(2) 电解精炼粗铜,粗铜做阳极,纯铜作阴极,含有铜离子的溶液做电解液,所以:X电极的材料纯铜;溶液中的铜离子发生还原反应: Cu2+ + 2e - = Cu;Y电极的材料是粗铜,金属铜失电子,发生氧化反应;Cu - 2e - = Cu2+;


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】现在,我们把无污染.无公害的食品叫做绿色食品。而最初,专家把绿色植物通过光合作用转化的食品叫做绿色食品,海洋提供的食品叫做蓝色食品,通过微生物发酵制得的食品叫做白色食品。根据最初的说法,下列属于绿色食品的是( )
A. 大米 B. 海带 C. 食醋 D. 食盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工业为人类解决粮食问题做出了巨大贡献.一定条件下,在密闭容器中进行合成氨反应:N2(g)+3H2(g)2NH3(g),当正、逆反应速率相等且不等于零时,下列说法不正确的是( )
A. N2、H2完全转化为NH3 B. N2、H2、NH3在容器中共存
C. 反应已达到化学平衡状态 D. N2、H2、NH3的浓度不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨的合成是目前普遍使用的人工固氮方法。
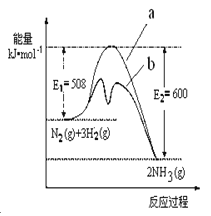
(1) 根据图提供的信息,写出该反应的热化学方程 ,下图的曲线中 (填“a” 或“b”)表示加入铁触媒的能量变化曲线。
(2) 在恒容容器中,下列描述中能说明上述反应已达平衡的是
A.3v(H2)正=2v(NH3)逆
B.单位时间内生成n mol N2的同时生成2n molNH3
C.容器内气体的密度不随时间的变化而变化
D.容器内压强不随时间的变化而变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子一定能大量共存的是 ( )
A.在含有大量Al3+的无色溶液中:Cu2+、Na+、Cl-、SO42-
B.在含有大量H+ 的 溶液中:Na+、K+、CO32-、NO3-
C.在强酸的溶液中:NH4+、Na+、SO42-、Cl-
D.在滴加石蕊显蓝色的溶液中:K+、Cu2+、Cl-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃时部分弱电解质的电离平衡常数数据如下表:
化学式 | CH3COOH | H2CO3 | HClO | |
平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
回答下列问题:
(1) 物质的量浓度均为0.1mol·L一1的四种溶液:a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3,pH由小到大的排列顺序是___________ (用字母表示)
(2) 常温下,0.1mol·L—1的CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是_______ (填序号)
A.c(H+) B.c(H+)/c(CH3COOH)
C.c(H+)·c(OH—) D.c(OH-)/c(H+)
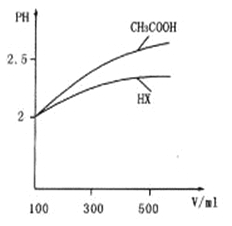
(3) 体积均为l00mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数_______ (填“>”、“<”或“=”)CH3COOH的电离平衡常数。
(4) 25℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中:
① c(CH3COO—)—c(Na+)=_______ mol·L—1(填精确值)
② c(CH3COO-)/c(CH3COOH)=_______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H、N、O、Na、S、Cl都是中学化学中的常见元素,根据题意回答与这些元素有关的问题:
(1)画出Na原子结构示意图_______,Na2O2可用作供氧剂,其电子式为_______。
(2)Cl2是一种大气污染物,装有液氯的钢瓶上应贴的标签是_______(填编号)。

氯气泄漏可用NaHSO3溶液来处理,写出相关的离子反应方程式_____________。
(3)25C时,利用pH试纸测得0.1mol/L氨水的pH约为11,则可以估算出氨水的电离常数约为_____;向10mL此溶液中通入少量氨气,忽略溶解过程中溶液温度和体积的微小变化,溶液中![]() 将_______(填“增大” “减小”或“无法确定”)。
将_______(填“增大” “减小”或“无法确定”)。
(4)有两种化合物同时含有上述六元素中的四种元素。将这两种化合物的溶液混合后,恰好完全反应,生成物之一M仍含有这四种元素,该反应的离子方程式为______________。若M溶液的pH =5,则由水电离出的c(H+)=_______mol/L,该溶液离子浓度由大到小的顺序为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验现象所得出的结论正确的是
选项 | 实验现象 | 实验结论 |
A | 将铝片分别投入浓、稀硝酸中,前者无明显现象,后者反应剧烈 | 稀硝酸的氧化性比浓硝酸的强 |
B | 滴有酚酞的Na2CO3溶液中加入BaCl2溶液,红色变浅 | Na2CO3溶液中存在水解平衡 |
C | 某溶液中滴加过量氨水产生白色沉淀且不溶解 | 该溶液中一定含有Mg2+ |
D | 溴水中通入SO2,溴水褪色 | SO2具有漂白性 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,第一种是混合物,第二种是盐,第三种是酸的是
A. 空气、硫酸铜、硫酸 B. 水、空气、纯碱
C. 食盐水、硝酸、烧碱 D. 氧化铁、胆矾、熟石灰
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com