
【题目】下列实验基本操作或实验注意事项中,主要是出于实验安全考虑的是
A.过滤时玻璃棒不能在漏斗内搅拌 B.可燃性气体的验纯
C.使用分液漏斗前要检验是否漏液 D.胶头滴管不能交叉混用
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】葡萄中含有酒石酸。酒石酸的化学分析如下:①相对分子质量为150,完全燃烧后只生成CO2和H2O,分子中C、H质量分数分别为w(C)=32%和w(H)=4%;②1 mol酒石酸与足量的NaHCO3反应放出44.8 L CO2,与足量的Na反应放出44.8 L H2(气体体积均已折算为标准状况);③核磁共振氢谱表明该分子中只有三种化学环境不同的氢原子。已知同一个碳原子上连接两个羟基时不稳定,会转化为其他物质。回答下列问题:
(1)酒石酸的分子式为_________________
(2)酒石酸的结构简式为_____________________
(3)有机物M是酒石酸的一种同分异构体,且M与酒石酸含有的官能团种类和数目均相同,写出M的结构简式:_____________________。M的核磁共振氢谱图中有_______组吸收峰。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将0.05 mol Na2CO3固体溶于水配成100mL溶液,向溶液中加入下列物质。有关结论正确的是( )
加入的物质 | 结论 | |
A | 50mL 1 mol·L-1H2SO4 | 反应结束后,c(Na+)=c(SO42-) |
B | 0.05molCaO | 溶液中 |
C | 50mL H2O | 由水电离出的c(H+)·c(OH—)不变 |
D | 0.1molNaHSO4固体 | 反应完全后,溶液pH减小,c(Na+)不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在甲乙两烧杯溶液中,分别含有大量的Cu2+、K+、H+、Cl-、CO32-、OH-六种离子中的三种,已知乙烧杯中的溶液呈无色,则乙烧杯的溶液中大量存在的离子是
A.Cu2+、H+、Cl-
B.Cl-、CO32-、OH-
C.K+、H+、Cl-
D.K+、OH-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《中华人民共和国安全生产法》指出安全生产工作应当以人为本,坚持安全发展、预防为主、综合治理的方针.下列做法不正确的是( )
A.面粉生产车间应严禁烟火
B.NH3泄露时向空中喷洒水雾
C.含Cl2的尾气用碱溶液处理后再排放
D.金属钠失火时应立即用大量冷水扑灭
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】意大利罗马大学的Fulvio Cacace等人获得极具理论研究意义的N4分子。N4分子结构如图所示,已知断裂1mol N-N吸收167kJ热量,生成1molN≡N放出942kJ热量.根据以上信息和数据,下列说法正确的是( )

A. N4属于一种新型的化合物
B. N4的沸点比P4(白磷)的高
C. 理论上可以将N4转化为N2的反应设计成原电池
D. 1mol N4所含有的能量比2mol N2所含有的能量高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。
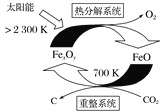
(1)科学家提出由CO2制取C的太阳能工艺如上图所示。
①若“重整系统”发生的反应中![]() =6,则FexOy的化学式为________。
=6,则FexOy的化学式为________。
②“热分解系统”中每分解1molFexOy,转移电子的物质的量为________。
⑵工业上用CO2和H2反应合成甲醚。已知:
CO2(g)+3H2(g)===CH3OH(g)+H2O(g) ΔH1=-53.7kJ·mol-1
CH3OCH3(g)+H2O(g)===2CH3OH(g) ΔH2=+23.4kJ·mol-1
则2CO2(g)+6H2(g)===CH3OCH3(g)+3H2O(g) ΔH3=________kJ·mol-1。
①一定条件下,上述合成甲醚的反应达到平衡状态后,若改变反应的某一个条件,下列变化能说明平衡一定向正反应方向移动的是________(填字母)。
a. 逆反应速率先增大后减小 b.H2的转化率增大
c.反应物的体积百分含量减小 d.容器中的![]() 值变小
值变小
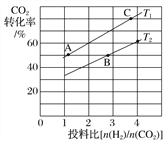
②在某压强下,合成甲醚的反应在不同温度、不同投料比时,CO2的转化率如下图所示。T1温度下,将6molCO2和12molH2充入2L的密闭容器中,5min后反应达到平衡状态,则0~5min内的平均反应速率v(CH3OCH3)=__________;KA、KB、KC三者之间的大小关系为____________。
(3)常温下,用氨水吸收CO2可得到NH4HCO3溶液,在NH4HCO3溶液中,c(NH4+)________(填“>”、“<”或“=”)c(HCO![]() );反应NH
);反应NH![]() +HCO
+HCO![]() +H2ONH3·H2O+H2CO3的平衡常数K=__________。(已知常温下NH3·H2O的电离平衡常数Kb=2×10-5,H2CO3的电离平衡常数K1=4×10-7,K2=4×10-11)
+H2ONH3·H2O+H2CO3的平衡常数K=__________。(已知常温下NH3·H2O的电离平衡常数Kb=2×10-5,H2CO3的电离平衡常数K1=4×10-7,K2=4×10-11)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 锌与稀硫酸反应:Zn+H+===Zn2++H2↑
B. 铜粉与稀硝酸的反应:Cu+2H+===Cu2++H2↑
C. 氢氧化镁与盐酸反应:H++OH-===H2O
D. 硝酸银溶液与氯化钠溶液反应:Ag++Cl-===AgCl↓
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com