
| A、向含有1 mol KAl(SO4)2的溶液中加入Ba(OH)2溶液至沉淀质量最大时,沉淀的总的物质的量为2.5 mol |
| B、FeCl2、Fe(OH)3均可通过化合反应制得 |
| C、由水电离的c(H+)为10-13mol/L的溶液,Na+、NO3-、SO42-、I-一定能大量共存 |
| D、可以用浓盐酸酸化的KMnO4溶液与H2O2混合,以证明H2O2具有还原性:2MnO4-+8H++5H2O2=2Mn2++5O2↑+8H2O |


 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:

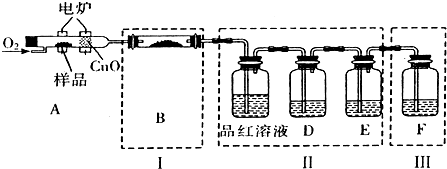
| A、乙醇在反应中发生了氧化反应 |
| B、为增强检测效果,加入盐酸酸化重铬酸钾溶液 |
| C、每1 mol乙醇参与反应转移电子物质的量为4mol |
| D、乙醇汽油是一种较清洁能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3.36L |
| B、6.72 L |
| C、8.96 L |
| D、4.48 L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验 试剂/mL | 甲 | 乙 | 丙 | 丁 |
| 4mol/L H2SO4 | 20 | V1 | V2 | V3 |
| 饱和CuSO4溶液 | 0 | 2.5 | V4 | 10 |
| H2O | V5 | V6 | 8 | 0 |
| A、实验甲产生气泡的速率最快 |
| B、V1<V2<V3<20 |
| C、V4=V5=10 |
| D、V6=7.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.5 mol/L NaHSO4与0.5 mol/L Ba(OH)2混合至溶液呈中性:Ba2++OH-+SO42-+H+═BaSO4↓+H2O |
| B、向2 mol/L Fe(NO3)2(aq)中滴加少量氢碘酸:3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O |
| C、向20 mL0.15 mol/L氢碘酸中通入224 mL Cl2(标准状况):2HI+Cl2═2H++I2+2Cl- |
| D、向40 mL 0.5 mol/L NaOH(aq)中通入224 mL CO2(标准状况):2OH-+CO2═CO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1000mL,212g |
| B、950mL,543.4g |
| C、任意规格,572g |
| D、500mL,286g |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

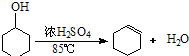
| 密度 (g/cm3) | 熔点 (℃) | 沸点 (℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com