
【题目】下列说法正确的是 ( )
A. 纤维素和淀粉遇碘水均显蓝色
B. 蛋白质、乙酸和葡萄糖均属电解质
C. 溴乙烷与NaOH乙醇溶液共热生成乙烯
D. 乙酸乙酯和食用植物油均可水解生成乙醇
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列对应关系错误的是( )
化学性质 | 实际应用 | |
A | Al2(SO4)3和小苏打反应 | 泡沫灭火器灭火 |
B | 铁比铜金属性强 | 刻制印刷电路板 |
C | 次氯酸盐具有氧化性 | 作杀菌消毒剂 |
D | 二氧化硫具有漂白性 | 漂白纸浆 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上有一种方法有效地开发利用CO2,是用CO2来生产燃料甲醇。为探究反应原理,进行如下实验,在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g);△H=-49.0kJ/mol.测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g);△H=-49.0kJ/mol.测得CO2和CH3OH(g)的浓度随时间变化如图所示。
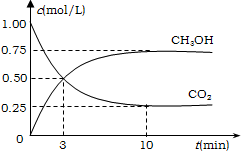
(1)从反应开始到平衡,氢气的平均反应速率v(CO2)= ________mol/(Lmin);
(2)氢气的转化率= ________;
(3)求此温度下该反应的平衡常数K=________;
(4)下列措施中能使平衡体系中n(CH3OH)/n(CO2)增大的是________
A.将H2O(g)从体系中分离出去
B.充入He(g),使体系压强增大
C.升高温度
D.再充入1mol CO2和3mol H2
(5)当反应达到平衡时,CO2的物质的量浓度为c1,然后向容器中再加入一定量CO2,待反应再一次达到平衡后,CO2的物质的量浓度为c2,则c1________ c2(填>、<、=)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用MnO2、KOH及KClO3为原料制取高锰酸钾的实验流程如下:
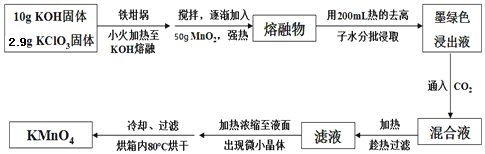
回答下列问题:
(1)实验中采用 (填“铁坩埚”或“瓷坩埚”)加热KOH和KClO3固体混合物。
(2)熔融时,MnO2转化为K2MnO4,KClO3转化为KCl,其反应的化学方程式为 。
(3)几种物质的溶解度曲线如图所示。
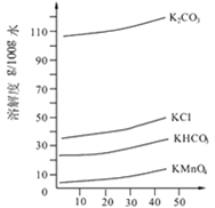
①通入CO2至pH为10~11,K2MnO4转化为KMnO4和MnO2。其反应的离子方程式为 。
②不能通入过量CO2的原因是 。
(4)趁热过滤的目的是 ;用冷水洗涤KMnO4晶体较好的原因是 。
(5)计算经过上述转化,最多可制得KMnO4的质量为 (结果保留2为小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组对H2O2的分解做了如下探究.下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将质量相同的粉末状和块状的MnO2分别加入盛有15ml 5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
MnO2 触摸试管情况 观察结果 反应完成所需的时间
粉末状 很烫 剧烈反应,带火星的木条复燃 3.5min
块状 微热 反应较慢,火星红亮但木条未复燃 30min
(1)写出上述实验中发生反应的化学方程式: .
(2)实验结果表明,催化剂的催化效果与 有关.
(3)某同学在10mL H2O2 溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的反应速率最慢的是 .
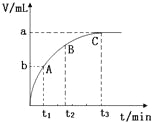
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com