
(18分)过氧化钠(Na2O2)是中学常见物质,常见的过氧化物还包括过氧化钙(CaO2)。已知:过氧化钠与CO2反应有气体生成,而将SO2通入过氧化钠粉末中也有气体生成。有人提出CO2、SO2与过氧化钠的反应原理相同,但也有人提出SO2具有较强的还原性,CO2无强还原性,反应原理不相同。据此设计如下实验操作进行判断。
实验一:向一定量的过氧化钠固体中通入足量的SO2,取反应后的固体进行实验探究,以证明过氧化物与SO2反应的特点。
(1)提出假设:
假设1:反应后固体中只有________,证明SO2未被氧化;
假设2:反应后固体中只有________,证明SO2完全被氧化;
假设3:__________________________证明______________________。
实验探究:
实验二:通过测量气体的体积判断发生的化学反应,实验装置如下:
(2)试剂A可以选用________,试剂B的作用是________。
(3)实验测得装置C中过氧化钠质量增加了m1 g,装置D质量增加了m2 g,装置E中收集到的气体为V L(已换算成标准状况下),用上述有关测量数据判断,SO2未被氧化、完全被氧化的V-m1关系式。
未被氧化:____________,完全被氧化:____________。
(4)若SO2完全被氧化,写出反应的化学方程式: __________________________
(1)Na2SO3 Na2SO4 Na2SO3和Na2SO4的混合物 SO2被部分氧化
(2)浓H2SO4 吸收未反应的SO2 (3)V=7m1/30 V=0
(4)SO2+Na2O2 ==Na2SO4
解析试题分析:(1)如果生成的固体中只有亚硫酸钠,则SO2未被氧化;如果生成的固体只有硫酸钠,则全部被氧化;如果既有亚硫酸钠,也有硫酸钠,则SO2是部分被氧化。
(2)根据装置可知,A是制取SO2的。但由于生成的SO2中含有水蒸气,而水蒸气也能和过氧化钙反应,所以装置B中的试剂应该是浓硫酸,用来干燥SO2;由于SO2和过氧化钙的反应中,SO2是过量的,所以为了防止SO2对反应中生成的气体的干扰,则装置D中应该盛放碱石灰,用来吸收未反应的SO2。
(3)如果SO2没有被氧化,则反应式是2Na2O2+2SO2=2Na2SO3+O2,所以生成的氧气体积是V=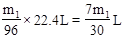 ;如果是完全被氧化,则生成气体是0,即反应的方程式为Na2O2+SO2===Na2SO4。
;如果是完全被氧化,则生成气体是0,即反应的方程式为Na2O2+SO2===Na2SO4。
考点:化学实验
点评:本题主要掌握Na2O2与具有还原性物质反应时的规律。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:宁夏银川一中2011-2012学年高二下学期期中考试化学试题 题型:022
硫化物通常有“废物”之称.硫化物据其溶解性可以分三类:
①易溶于水的有K2S、Na2S、(NH4)2S等;
②易溶于非氧化性强酸、不溶于水的有FeS、ZnS;
③大部分的硫化物既不溶于水也不溶于非氧化性强酸,如HgS、Ag2S、CuS、Cu2S.其中,Ag2S、CuS、Cu2S能溶于硝酸发生氧化还原反应,而HgS只能溶于王水(硝酸与盐酸的混合液).氢硫酸溶液中存在下列平衡:
H2S(1)K2S溶液显________性,原因________(用离子方程式表示)K2S溶液中离子浓度由大到小顺序________
(2)推测将硫化氢通入硫酸铜溶液中生成硫酸的原因是________
(3)在氢硫酸溶液中改变下列条件,使溶液中.c(OH-)、c(S2-)都增大的是________
A.加入少量的漂白粉
B.通入氨气
C.加入少量过氧化钠粉末
D.加入少量硝酸银溶液
(4)已知在常温下FeS的Ksp=6.25×10-18,H2S饱和溶液中c(H+)与cS2-)之间存在如下关系:c2(H+)·(S2-)=1.0×10-22.在该温度下,将适量FeS入硫化氢饱和溶液中,欲使溶液中(Fe2+)为1 mol/L,应调节溶液的c(H+)为________.
查看答案和解析>>
科目:高中化学 来源:2012-2013学年河南省高三第五次月考化学试卷(解析版) 题型:实验题
(18分)过氧化钠(Na2O2)是中学常见物质,常见的过氧化物还包括过氧化钙(CaO2)。已知:过氧化钠与CO2反应有气体生成,而将SO2通入过氧化钠粉末中也有气体生成。有人提出CO2、SO2与过氧化钠的反应原理相同,但也有人提出SO2具有较强的还原性,CO2无强还原性,反应原理不相同。据此设计如下实验操作进行判断。
实验一:向一定量的过氧化钠固体中通入足量的SO2,取反应后的固体进行实验探究,以证明过氧化物与SO2反应的特点。
(1)提出假设:
假设1:反应后固体中只有________,证明SO2未被氧化;
假设2:反应后固体中只有________,证明SO2完全被氧化;
假设3:__________________________证明______________________。
实验探究:
实验二:通过测量气体的体积判断发生的化学反应,实验装置如下:

(2)试剂A可以选用________,试剂B的作用是________。
(3)实验测得装置C中过氧化钠质量增加了m1 g,装置D质量增加了m2 g,装置E中收集到的气体为V L(已换算成标准状况下),用上述有关测量数据判断,SO2未被氧化、完全被氧化的V-m1关系式。
未被氧化:____________,完全被氧化:____________。
(4)若SO2完全被氧化,写出反应的化学方程式: __________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
硫化物通常有“废物”之称。硫化物据其溶解性可以分三类: ① 易溶于水的有 K2S 、Na2S 、(NH4)2S 等; ② 易溶于非氧化性强酸、不溶于水的有 FeS 、 ZnS ; ③大部分的硫化物既不溶于水也不溶于非氧化性强酸,如 HgS 、 Ag2S 、 CuS 、 Cu2S 。其中,Ag2S、 CuS 、 Cu2S 能溶于硝酸发生氧化还原反应,而 HgS只能溶于王水(硝酸与盐酸的混合液)。氢硫酸溶液中存在下列平衡:
H2S ![]() H ++ HS-, HS-
H ++ HS-, HS- ![]() H + + S2-。
H + + S2-。
(1)K2S溶液显___________性,原因______________________(用离子方程式表示)
K2S溶液中离子浓度由大到小顺序____________________________________________
(2)推测将硫化氢通入硫酸铜溶液中生成硫酸的原因是___________________________
(3)在氢硫酸溶液中改变下列条件,使溶液中。c(OH-)、c(S2-)都增大的是______
A.加入少量的漂白粉 B.通入氨气
C.加入少量过氧化钠粉末 D.加入少量硝酸银溶液
(4)已知在常温下 FeS 的Ksp=6.25 ×10-18,H2S饱和溶液中c(H+)与c S2-)之间存在如下关系:c2(H+)·(S2-)= 1.0×10-22 。在该温度下,将适量FeS 入硫化氢饱和溶液中,欲使溶液中(Fe2+)为 lmol/L,应调节溶液的c(H十)为__________________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com