
科目:高中化学 来源:不详 题型:单选题
| A.用托盘天平称取5.5 g KCl固体 |
| B.在酸碱中和滴定实验中,量取20. 00 mL待测NaOH溶液用20mL量筒 |
| C.将干燥的pH试纸浸入某溶液一会儿后取出,与标准比色卡比较以测定该溶液的pH |
| D.配制0.1 mol·L-1的硫酸溶液时,将量取的浓硫酸放入容量瓶中加水稀释 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.滴定时,装NaOH溶液的锥形瓶未用NaOH溶液润洗 |
| B.酸式滴定管用蒸馏水洗后,用标准盐酸润洗 |
| C.滴定前,酸式滴定管尖嘴处有气泡,而在滴定后气泡消失 |
| D.配制NaOH溶液时,NaOH固体中混有少量KOH固体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
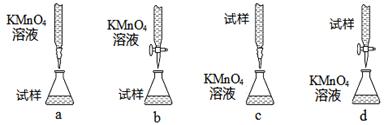
| 滴定次数 实验数据 | 1 | 2 | 3 |
| V(样品)/mL | 20.00 | 20.00 | 20.00 |
| V(KMnO4)/mL(初读数) | 0.00 | 0.20 | 0.00 |
| V(KMnO4)/mL(终读数) | 15.85 | 15.22 | 14.98 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用玻璃棒蘸取溶液,点在湿润的pH试纸上测定其pH |
| B.凡是能自发进行的化学反应,一定是△H<0、△S>0 |
| C.“中和滴定”实验中,容量瓶和锥形瓶用蒸馏水洗净后即可使用,滴定管和移液管用蒸馏水洗净后,须经润洗后方可使用 |
| D.Ksp与难溶电解质的性质、温度、溶液中的离子浓度等因素有关 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com