
【题目】在塑料袋中放一个成熟的苹果,再放些青香蕉,将袋口密封.两天后,发现青香蕉成熟了.导致青香蕉成熟的物质是成熟苹果释放出的( )
A.C2H4
B.CH3COOH
C.C6H6
D.CH3CH2OH
科目:高中化学 来源: 题型:
【题目】CO2、CS2、COS是由C、O、S三种元素形成的结构相似的化合物。
(1)下列能说明碳、硫两种元素非金属性相对强弱的是_____________(填序号)
A.亚硫酸溶液加入Na2CO3溶液中,产生气泡
B.氧化性:浓H2SO4>H2CO3
C.CS2中碳元素为+4价,硫元素为—2价
D.SO2有较强还原性,而CO2无还原性
(2)羰基硫(COS)可作为一种熏蒸剂,能防止某些昆虫、线虫的危害。
① 羰基硫的结构式为:________________。沸点:CO2_________COS(填“大于”或“小于”),说明原因_____________________。
②下列有关羰基硫的推测肯定不正确的是_________________
A.COS分子中,所有原子都满足8电子的稳定结构
B.COS分子是含有极性键的非极性分子
C.COS分子中三个原子处于同一直线上
D.COS可能在O2中燃烧
③ 羰基硫(COS)用氢氧化钠溶液处理及利用的过程如下图:

已知A是一种盐,则A的化学式为________;气体单质a为____________________.
(3)在恒容密闭容器中,CO和H2S混合加热生成羰基硫的反应为CO(g)+H2S(g)![]() COS(g)+H2(g),反应前CO和H2S的物质的量均为10mol,平衡后CO的物质的量为8mol,回答下列问题:
COS(g)+H2(g),反应前CO和H2S的物质的量均为10mol,平衡后CO的物质的量为8mol,回答下列问题:
①升高温度,H2S浓度增加,表明该反应是__________________反应(填“放热”或“吸热”)。
②平衡时,继续通入CO10mol和H2S10mol,一段时间后再次达到平衡,此时H2S的转化率_____(填“增大”“减小”或“不变”)
(4)若反应在恒容密闭容器中进行,能说明该反应已达到平衡状态的是____________
A.容器内气体密度保持不变
B.CO、H2S、COS、H2的浓度均不再变化
C.c(H2)=c(H2S)
D.v(H2)正=v(H2S)逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究大气中含硫化合物和含碳化合物的转化对环境保护具有重要意义。
(1)SO2的大量排放会引起严重的环境问题是 ,潮湿条件下,写出大气中SO2转化为HSO3-的方程式 ;
(2)土壤中的微生物可将大气中H2S经两步反应氧化成SO42-,两步反应的能量变化示意图如下:

1mol H2S(g)全部氧化成SO42-(aq)的热化学方程式为 ;
(3)SO2是工业制硫酸的原料之一,一定温度下,向容积为2L的密闭容器中充入一定量的SO2和O2,发生反应:2SO2(g)+O2(g)![]() 2SO3(g),过程中测定的部分数据见下表:
2SO3(g),过程中测定的部分数据见下表:
时间/min | n(SO2)/mol | n(O2)/mol |
0 | 0.10 | 0.05 |
4 | 0.04 | 0.02 |
6 | 0.02 | |
8 | 0.01 |
①反应在0-4min内的平均速率为v(SO2)= ;
②此温度下该反应的化学平衡常数K= ;
③8min时,维持温度不变,向反应容器中再通入0.02mol SO2(g)和0.01mol O2(g),重新达到平衡时混合气体中SO2的百分含量将 (填“减小”、“增大”或“不变”)。
(4)科学家用氮化镓材料与铜组装如下图的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4的反应。

写出铜电极表面的电极反应式 ,为提高该人工光合系统的工作效率,可向装置中加入少量 (填“盐酸”或“硫酸”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是有关实验操作的步骤和做法,正确的是( )
A. 粗盐提纯操作的顺序是:溶解、过滤、蒸发、洗涤
B. 实验室制取氧气完毕后,应先停止加热,再取出导管
C. 不慎将浓硫酸洒在桌上,应先用烧碱溶液中和,再用湿布抹净
D. 用试管夹夹持试管时,把试管夹从试管底部往上套,夹在试管中上部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机物的叙述不正确的是
A. 甲烷、乙醇、乙酸和酯类都可以发生取代反应
B. 乙烯和苯都能使溴水褪色,但颜色的原因不同
C. 石油催化裂化的主要目的是提高芳香烃的产量
D. 纤维素和蛋白质都是能发生水解反应的高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃,1.01×105Pa时,反应:2N2O5(g) = 4NO2(g) +O2(g) △H = + 56.76 kJ·mol-1,能自发进行的原因是
A. 是吸热反应 B. 是放热反应 C. 是熵减少的反应 D. 熵增大效应大于能量效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 酸化高锰酸钾溶液时可以用盐酸酸化
B. 金属钠着火时不能用泡沫灭火器灭火
C. 氢氧化铁胶体的电泳实验,证明了氢氧化铁胶体带电荷
D. 能与碱反应生成盐和水的氧化物一定是酸性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
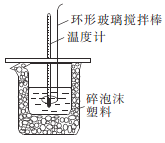
(1)环形玻璃搅拌棒的作用是___________________。
(2)中和反应放出的热量会造成少量盐酸在反应中挥发,则测得的中和热的数值________(填“偏大”、“偏小”或“不变”)。
(3)该实验小组做了三次实验,每次取溶液各50 mL,并将实验数据记录如下:

已知盐酸、NaOH溶液的密度与水相同,中和后生成的溶液的比热容c=4.18×10-3kJ/(g.℃),则该反应的中和热△H=__________。
(4)在中和热测定实验中,测量起始温度时需要两个温度计,如果只用一个温度计测量,则测得的中和热的数值___________(填“偏大”、“偏小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com