
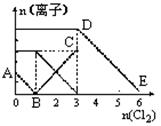
| A���߶�BC����Fe3+���ʵ����ı仯��� |
| B��ԭ�����Һ��n(FeBr2)��3mol |
| C����ͨ��Cl22molʱ����Һ���ѷ��������ӷ�Ӧ�ɱ�ʾΪ�� 2Fe2++2I-+2C12��2Fe3++I2+4Cl- |
| D��ԭ��Һ��n(Fe2+):n(I-):n(Br-)��3:1: 2 |
 Happy holiday���ּ��������ҵ�㶫���������ϵ�д�
Happy holiday���ּ��������ҵ�㶫���������ϵ�д� ���������������Բ��������ϵ�д�
���������������Բ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 ���������ԣ�A2 > D2
���������ԣ�A2 > D2�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| ��� | ��Ӧ�� | ���� |
| �� | KMnO4 ��H2O2 ��H2SO4 | K2SO4 ��MnSO4 ������������ |
| �� | Cl2 ��FeBr2 | FeCl3��FeBr3 |
| �� | MnO4�� ������������ | Cl2 ��Mn2+ ������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2Fe2++I2�͢� Br2+2Fe2+
2Fe2++I2�͢� Br2+2Fe2+ 2Fe3++ 2Br�������ж����ӵĻ�ԭ�Դ�ǿ������˳���ǣ� ��
2Fe3++ 2Br�������ж����ӵĻ�ԭ�Դ�ǿ������˳���ǣ� ��| A��Br����Fe2+��I�� | B��I����Fe2+��Br�� |
| C��Br����I����Fe2+ | D��Fe2+��I����Br�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��H2O2+ H2SO4��SO2��+ O2��+2 H2O |
| B��2I�C +2Fe3����I2+2 Fe2�� |
| C��2Fe3��+ SO2 +2H2O��2Fe2��+SO42�C +4H�� |
| D��SO2 +2 H2O+ I2��H2SO4+2HI |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ClO3����BrO3����IO3����Cl2 | B��BrO3�� ��Cl2��C1O3����IO3�� |
| C��BrO3����ClO3����Cl2��IO3�� | D��Cl2��BrO3����C1O3����IO3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��X��Z��Y��W | B��Z��W��X��Y |
| C��Z��Y��X��W | D��Z��X��Y��W |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com