
 һ���¶��½�1 mol H2��2 mol I2����ij2L�ܱ������У�������Ӧ��H2 ��g��+ I2��g��
һ���¶��½�1 mol H2��2 mol I2����ij2L�ܱ������У�������Ӧ��H2 ��g��+ I2��g�� ![]() 2HI��g������H <0�����ﵽƽ�⣬HI���������
2HI��g������H <0�����ﵽƽ�⣬HI���������![]() ��ʱ��(t)�仯��ͼ(I) ��ʾ�����ı䷴Ӧ������
��ʱ��(t)�仯��ͼ(I) ��ʾ�����ı䷴Ӧ������![]() �ı仯��ͼ(��)��ʾ����ı�����������ǣ�
�ı仯��ͼ(��)��ʾ����ı�����������ǣ�
A�����º��������£������ʵ�����
B�����������£���С��Ӧ�������
C�����������£�����Ӧ�������
D�����������£����߷�Ӧ��ϵ�¶�
D
���⿼�黯ѧƽ��ԭ����Ӧ�ã��ؼ�������ȷ��ɳ����ԭ����Ӧ�÷�Χ�������ʵ�������ƽ�ⲻ�ƶ���A����ͼ�����壻���������£���С��Ӧ���������ѹǿ�������ƽ�ⲻ�ƶ���B����ͼ�����壻���������£�����Ӧ���������ѹǿ��С�������ƽ�ⲻ�ƶ���C����ͼ�����壻����Ӧ���ȣ����������£����߷�Ӧ��ϵ�¶ȣ�ƽ�����淴Ӧ�����ƶ�����(HI)��С����Ӧ���ʼӿ죬ƽ��ʱ�����̣�D����ͼ�����塣


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ�����е�һ��ѧ2011��2012ѧ��߶���ѧ�����л�ѧ���� ���ͣ�013
|
��һ���¶��½���1 mol��CO��ˮ���������ܱյ������з�Ӧ��CO(g)��H2O(g)CO2(g)��H2(g)�ﵽƽ����CO2Ϊ0.6 mol����ͨ��4 molˮ�������ﵽƽ���CO2�����ʵ���Ϊ | |
| [����] | |
A�� |
����0.6 mo |
B�� |
����1 mol |
C�� |
����0.6 mol��1 mol |
D�� |
����1 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ��㶫ʡ��Զ�и�����ѧ����ĩ������ۻ�ѧ�Ծ��������棩 ���ͣ�������
��Դ��ȱ���������ٵ��ش����⡣�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ������˼״�����Ϊ21���͵�����ȼ�ϡ�
��1����֪�ڳ��³�ѹ�£�
�� 2CH3OH(l)+3O2(g)
2CO2(g)+4H2O(g) ��H= ��1275.6 kJ��mol��1
�� H2O(l) H2O(g)
��H=+ 44.0 kJ.mo��1
д����ʾ�״�ȼ���ȵ��Ȼ�ѧ����ʽ ��
��2����ҵ����CO����ȼ�ϼ״���һ�������·�����Ӧ��CO(g)+2H2(g) CH3OH(g)��ͼ1��ʾ��Ӧ�������ı仯��ͼ2��ʾһ���¶��£������Ϊ2L���ܱ������м���4mol H2��һ������CO��CO��CH3OH(g)��Ũ����ʱ��仯ͼ��
CH3OH(g)��ͼ1��ʾ��Ӧ�������ı仯��ͼ2��ʾһ���¶��£������Ϊ2L���ܱ������м���4mol H2��һ������CO��CO��CH3OH(g)��Ũ����ʱ��仯ͼ��

���ڡ�ͼ1���У����� ���a����b������ʾʹ���˴�����
�����жϸ÷�Ӧ�ڡ�ͼ2�������������Ƿ��Ѵﻯѧƽ��״̬�������� ����˫ѡ��
A��������ѹǿ���� B����ϵ���ܶȲ���ʱ��ı�
C��v��(H2)=2v��(CH3OH) D��CO��H2�����ʵ����ıȲ���ʱ��ı�
�ۼ�����¶���CO(g)+2H2(g) CH3OH(g)�Ļ�ѧƽ�ⳣ��K=
��
CH3OH(g)�Ļ�ѧƽ�ⳣ��K=
��
�����ڡ�ͼ3���л���ƽ��ʱ�״��ٷֺ����������꣩���¶ȣ������꣩�仯�����ߣ�Ҫ��ѹǿ��ͬ��2�����ߣ��������ϱ��P1��P2����P1<P2����
��3��CaSO4��һ�������ʣ���֪Ksp��CaSO4��=9.10��10��6���ֽ�c mol��L��1 CaCl2��Һ��2.00��10��2 mol��L��1 Na2SO4��Һ�����������ɳ�������c����Сֵ�� ���������3λ��Ч���֣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013��ӱ�ʡ�߶�9���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
һ�������½�2mol SO2��2mol SO3��������һ�̶��ݻ����ܱ������У�������Ӧ��
2SO2��O2 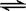 2SO3��ƽ��ʱSO3�������Ϊn ��������ͬ�¶��£��ֱ�������������������з�����ʼ���ʣ�ƽ��ʱSO3�������������n ������
�� ��
2SO3��ƽ��ʱSO3�������Ϊn ��������ͬ�¶��£��ֱ�������������������з�����ʼ���ʣ�ƽ��ʱSO3�������������n ������
�� ��
A��2 mol SO2 ��0.5mol O2 B��6 mol SO2 �� 1 mo+l O2 �� 2 SO3
C��4 mol SO2 �� 1 mol O2 D��3 mol SO2 �� 0��5 mol O2 �� 1 SO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ��ӱ�ʡ��һ�и߶�9���¿���ѧ�Ծ����������� ���ͣ���ѡ��
һ�������½�2mol SO2��2mol SO3��������һ�̶��ݻ����ܱ������У�������Ӧ��
2SO2��O2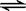 2SO3��ƽ��ʱSO3�������Ϊn ��������ͬ�¶��£��ֱ�������������������з�����ʼ���ʣ�ƽ��ʱSO3�������������n ������ �� ��
2SO3��ƽ��ʱSO3�������Ϊn ��������ͬ�¶��£��ֱ�������������������з�����ʼ���ʣ�ƽ��ʱSO3�������������n ������ �� ��
| A��2 mol SO2��0.5mol O2 | B��6 mol SO2�� 1 mo+l O2�� 2 SO3 |
| C��4 mol SO2�� 1 mol O2 | D��3 mol SO2�� 0��5 mol O2�� 1 SO3 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com