
| A. | 向氨水中加入氯化铵固体,会使溶液的pH减小 | |
| B. | 常温时,向CaCO3的饱和溶液中加入Na2CO3固体,则CaCO3的溶度积常数增大 | |
| C. | 常温时,把pH=1的醋酸溶液稀释10倍后,其pH大于2 | |
| D. | 稀释Na2CO3溶液,溶液中c(OH-)增大 |
分析 A.向溶液中加入相同离子的盐溶液,抑制弱电解质电离;
B.Ksp只与温度有关;
C.醋酸是弱电解质,在水溶液里存在电离平衡,加水稀释能促进醋酸电离;
D.Na2CO3溶液存在水解平衡:CO32-+H2O?HCO3-+OH-,稀释Na2CO3溶液,水解程度增大,但增加的氢氧根离子浓度量远不及溶液的体积增大量;
解答 解:A.向氨水中加入氯化铵固体,溶液中铵根离子浓度增大,抑制一水合氨电离,所以溶液的pH变化是变小,故A正确;
B.常温时,向CaCO3的饱和溶液中加入Na2CO3固体,CaCO3的溶解度减小,由于温度不变,所以溶度积常数不变,故B错误;
C.如果醋酸是强电解质,则pH=1的醋酸溶液加水稀释100倍,pH=2,实际上醋酸是弱电解质,所以稀释后pH<2,故C错误;
D.Na2CO3溶液加水稀释促进水解,OH-的物质的量增大,但增加的氢氧根离子浓度量远不及溶液的体积增大量,所以c(OH-)浓度减小,故D错误;
故选A.
点评 本题考查了平衡有关知识,注意电离平衡及水解平衡的影响因素,注意溶度积常数是温度的函数,与浓度无关,题目难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 在氧气中点燃细铁丝产生白色的烟 | |
| B. | 铁粉和硫粉混合加热生成黑色固体 | |
| C. | 纯铝在空气中放置会长出白毛 | |
| D. | 将铝片放入CuSO4溶液反应完全后,溶液由蓝色变为红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀盐酸 | B. | FeCl3 | C. | Fe(NO3)3 | D. | BaCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
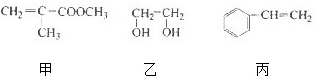
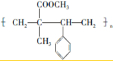 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol/L | B. | 2 mol/L | C. | 3 mol/L | D. | 20 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 沉淀中OH-的质量为(n-m)g | |
| B. | 反应过程中转移电子的物质的量为$\frac{n-m}{17}$mol | |
| C. | 标准状况下生成NO的体积为$\frac{2.24(n-m)}{51}$L | |
| D. | 与合金反应的硝酸的物质的量为($\frac{n-m}{51}$+$\frac{bv}{1000}$)mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com