
【题目】某有机物的结构简式如图所示,下列有关该物质的说法正确的是( )
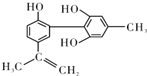
A.该物质的分子式为C16H18O3
B.该物质分子中的所有氢原子可能共平面
C.滴入KMnO4(H+)溶液,可观察到紫色褪去,能证明结构中存在碳碳双键
D.1mol该物质分别与浓溴水和H2反应时最多消耗Br2和H2分别为4mol、7mol
【答案】D
【解析】
试题分析:A.由有机物结构简式可知有机物的分子式为C16H16O3,故A错误;B.分子中含有甲基,具有甲烷的结构特征,则不可能所有的氢原子都在同一个平面上,故B错误;C.分子中能使酸性高锰酸钾褪色的有羟基、甲基和碳碳双键,则滴入KMnO4(H+)溶液,可观察到紫色褪去,不能证明结构中存在碳碳双键,故C错误;D.分子中含有3个酚羟基,能与溴发生取代的氢原子共有3个,含有1个碳碳双键,可与溴发生加成反应,分子中含有2个苯环、1个碳碳双键,都可与氢气发生加成反应,则1mol该物质分别与浓溴水和H2反应时最多消耗Br2和H2分别为4mol、7mol,故D正确;故选D。


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:
【题目】三个密闭容器中分别充入N2、H2、O2三种气体,以下各种情况下排序正确的是( )
A.当它们的温度和压强均相同时,三种气体的密度:ρ(H2)>ρ(N2)>ρ(O2)
B.当它们的温度和密度都相同时,三种气体的压强:p(H2)>p(N2)>p(O2)
C.当它们的质量和温度、压强均相同时,三种气体的体积:V(O2)>V(N2)>V(H2)
D.当它们的压强和体积、温度均相同时,三种气体的质量:m(H2)>m(N2)>m(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,当关闭K时,向A(恒容)中充入1molX、1molY,向B(带有活塞)中充入2molX、2molY,起始时,V(A)=V(B)=aL。在相同温度和催化剂存在的条件下,两容器中各自发生下列反应:2X(g)+2Y(g)![]() 3Z(g)+2W(g)△H<0,达到平衡(Ⅰ)时,V(B)=1.2aL,请回答:
3Z(g)+2W(g)△H<0,达到平衡(Ⅰ)时,V(B)=1.2aL,请回答:
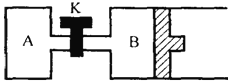
(1)B中X的转化率α(X)B为__________;
(2)A中W和B中W的物质的量比较:n(W)A_____n(W)B(填大于、小于、等于);
(3)打开K,过一段时间重新达平衡(Ⅱ)时,B的体积为______(用a的代数式表示,连通管中气体体积不计)。
(4)要使B容器恢复到原来反应前的体积,可采取的措施是_________。
A.升高温度 B.降低温度 C.充入稀有气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁铝合金质优体轻,又不易锈蚀,被大量用于航空工业、造船工业、日用化工等领域。下列关于镁铝合金性质的叙述中,正确的是( )
A.此合金的熔点比镁和铝的熔点都高
B.此合金能全部溶解于稀盐酸中
C.此合金能全部溶解于氢氧化钠溶液中
D.此合金的硬度比镁和铝的硬度都小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,分别将四块形状相同、质量均为7 g的铁片同时放入下列四种溶液中,产生气体速率最快的是( )
A.150 mL 2 mol·L-1盐酸 B.500 mL2mol·L-1硫酸
C.50 mL 3 mol·L-1盐酸 D.50 mL 18.4 mol·L-1硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.50ml,12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA
B.常温常压下4.4g乙醛所含σ键数目为0.7NA
C.向浓H2SO4中通入H2S气体,1mol浓H2SO4转移电子数一定是2 NA
D.2.0gH218O与D2O的混合物中所含中子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们.
(1)卤族元素位于周期表的 区;溴的价电子排布式为 .
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的.使氢氟酸分子缔合的作用力是 .
(3)请根据如表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是
氟 | 氯 | 溴 | 碘 | 铍 | |
第一电离能 | 1681 | 1251 | 1140 | 1008 | 900 |
(4)碘在水中的溶解度虽然小,但在碘化钾溶液中溶解度却明显增大这是由于溶液中发生下列反应I﹣+I2=I3﹣.I3﹣离子的中心原子周围σ键电子对对数为 ,孤电子对对数为 与KI3类似的,还有CsICl2等.已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列 式发生.
A.CsICl2═CsCl+ICl B.CsICl2═CsI+Cl2
(5)已知ClO2﹣为V形,中心氯原子周围有四对价层电子.ClO2﹣中心氯原子的杂化轨道类型为 ,写出一个ClO2﹣的等电子体 .
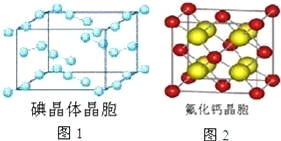
(6)图1为碘晶体晶胞结构.有关说法中正确的是 .
A.碘分子的排列有2种不同的取向,2种取向不同的碘分子以配位数4交替配位形成层结构
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中的碘原子间存在非极性键和范德华力
(7)已知CaF2晶体(见图2)的密度为ρg/cm3,NA为阿伏加德罗常数,棱上相邻的两个Ca2+的核间距为a cm,则CaF2的相对分子质量可以表示为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,0.1mol·L-1的某一元酸HA在水中有0.1%发生电离,下列说法不正确的是
A.该溶液pH=4
B.由HA电离出的c(H+)约为水电离的c(H+)的106倍
C.此酸的电离平衡常数约为1×10-7
D.升高温度,溶液的pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有机化合物A、B、C、D、E存在如图所示转化关系,且C能跟NaHCO3发生反应,C和D的相对分子质量相等,E为无支链的化合物.
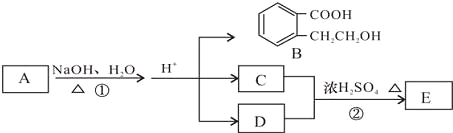
请回答下列问题:
(1)已知E的相对分子质量为102,其中碳、氢两种元素的质量分数分别为58.8%、9.8%,其余为氧,则E的分子式为 .
(2)B在一定条件下可以发生缩聚反应生成某高分子化合物,此高分子化合物的结构简式为 ![]() .
.
(3)D也可以由溴代烃F在NaOH溶液中加热来制取,写出此反应的化学方程式 .
(4)反应①的化学方程式 .
(5)B有多种同分异构体,请写出一种同时符合下列四个条件的结构简式: .
a.能够发生水解
b.能发生银镜反应
c.能够与FeCl3溶液显紫色
d.苯环上的一氯代物只有一种.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com