
【题目】细胞膜上一般不含( )
A. 胆固醇 B. 磷脂 C. 糖蛋白 D. 血红蛋白
科目:高中化学 来源: 题型:
【题目】铅及其化合物广泛用于蓄电池、机械制造、电缆护防等行业。
(1)用PbS熔炼铅的过程中会有如下反应发生:
2PbS(s)+3O2(g)=2PbO(s)+2SO2(g) △H=a kJ·mol-1
PbS(s) +2O2(g) =PbSO4(s) △H=b kJ·mol-1
PbS(s) +2PbO(s) =3Pb(s) +SO2(g) △H=c kJ·mol-1
写出PbS与PbSO4反应生成Pb和SO2的热化学方程式____________________。
(2)利用电解法也可制得金属铅。将PbO溶解在HCl和NaCl的混合溶液中,得到含[PbC14]2-的电解液。用惰性电极电解Na2PbCl4溶液制得金属Pb,装置如下图所示。

a电极的名称是__________,b电极的电极反应式为______________________,该生产过程中可以循环利用的物质是____________________。
(3)铅蓄电池是一种用途广泛的二次电池。铅蓄电池的电池反应通常表示如下:Pb+PbO2+2H2SO4![]() 2PbSO4 +2H2O。铅蓄电池充电时,二氧化铅电极应与外接电源的_________________(填“正极”或“负极”)相连接,该电极的电极反应式为________________________________。
2PbSO4 +2H2O。铅蓄电池充电时,二氧化铅电极应与外接电源的_________________(填“正极”或“负极”)相连接,该电极的电极反应式为________________________________。
(4)PbO2受热会随温度升高逐步分解。称取23.9g PbO2,将其加热分解,受热分解过程中固体质量随温度的变化如下图所示。

A点与C点对应物质的化学式分别为____________、_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下为中学化学中常见的物质:①Cu; ②1molL﹣1的FeCl3溶液; ③CuCl2溶液;④CO2;⑤H2SO4;⑥酒精;⑦CaCO3;⑧FeSO4
(1)以上物质中属于电解质的是;属于混合物的是 .
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入②的溶液,至液体呈透明的红褐色氢氧化铁胶体.则反应的化学方程式为;氢氧化铁胶体中分散质微粒的直径范围为nm;判断该胶体制备是否成功的方法是 .
(3)将②③⑧混合配制成浓度均为1molL﹣1的混合溶液100mL,加入一定量的铁粉,充分反应后,若铁粉无剩余,且有铜生成.则反应后的溶液中一定含有阳离子,可能含有阳离子,该阳离子在溶液中物质的量可能的存在范围是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正常生活的细胞内时刻进行着复杂有序的新陈代谢活动,而新陈代谢同两种物质密切相关,即酶和ATP,下列关于二者的叙述正确的是( )
A. 酶是活细胞产生的只能在活细胞中起作用的有机物
B. ATP水解掉两个磷酸余下部分可成为RNA的组成单位
C. ATP中的A为腺嘌呤
D. 酶能催化化学反应是因为酶能够为化学反应提供能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据氧化还原反应:2Ag+(aq)+Cu(s)Cu2+(aq)+2Ag(s)设计的原电池如图所示:

请回答下列问题:
(1)电极X的材料是________;电解质溶液Y是________;
(2)银电极为电池的________极,发生的电极反应为__________________;X电极上发生的电极反应为________________;
(3)外电路中的电子是从________电极流向________电极。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D和Cu五种金属片,将其分别用导线连接后浸入稀硫酸中(如图),每次实验时,通过灵敏电流计测出电子流动方向如下。

根据上述情况,回答下列问题:
(1)上述五种金属的活动性顺序是______________。
(2)在①中,Cu片上观察到的现象是_____________________。
(3)在②中,溶液中H+向金属片______________移动。
(4)在④中,两金属片上均无气泡放出。此时两金属片上的电极反应式分别为Cu:_____________________;B:____________________________。
(5)如果实验⑤用B、D,则导线中电流方向为_______(填“B→D”或“D→B”)。
(6)已知反应:Cu+2Fe3+Cu2++2Fe2+。请用下列试剂和材料,用如图所示装置,将此反应设计成原电池。
试剂:CuCl2溶液、FeCl3溶液、FeCl2溶液、双氧水、NaOH溶液
材料:Cu片、Fe片、石墨棒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由A、B、C、D四种金属按下表中装置图进行实验。
装置 |
|
|
|
现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是_______________。
(2)装置乙中正极的电极反应式是_______________。
(3)装置丙中溶液的pH________(填“变大”“变小”或“不变”)。
(4)四种金属活动性由强到弱的顺序是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.
请回答该实验中的问题.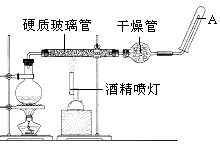
(1)写出该反应的反应方程式:
(2)如何检验该装置的气密性
(3)圆底烧瓶中盛装的水,该装置受热后的主要作用是;烧瓶底部放置了几片碎瓷片,碎瓷片的作用是 .
(4)酒精灯和酒精喷灯点燃的顺序是 , 为什么
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com