
 室温下,用0.1mol/L氨水分别滴定20.0mL、0.1mol/L的盐酸和醋酸,曲线如图所示,下列说法正确的( )
室温下,用0.1mol/L氨水分别滴定20.0mL、0.1mol/L的盐酸和醋酸,曲线如图所示,下列说法正确的( )| A. | I曲线表示的是滴定盐酸的曲线 | |
| B. | x=20 | |
| C. | 滴定过程中$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)}$的值逐渐减小 | |
| D. | 当I曲线和II曲线pH均为7时,一溶液中的c(Cl-)等于另一溶液中的c(CH3COO-) |
分析 A.0.1mol/L的盐酸的pH=1,结合滴定曲线开始时的pH来判断;
B.根据两者恰好反应生成氯化铵,氯化铵水解溶液呈酸性,要使溶液呈中性,则氨水应过量;
C.根据氨水的电离平衡常数只与温度有关以及c(OH-)在增大;
D.根据当I曲线和II曲线pH均为7时,在盐酸中,氨水过量,在醋酸中,氨水恰好反应,根据溶液中电荷守恒来解答.
解答 解:A.滴定开始时0.1mol/L盐酸pH=1,0.1mol/L醋酸pH>1,所以滴定盐酸的曲线是图Ⅱ,滴定醋酸的曲线是图Ⅰ,故A错误;
B.用0.1mol/L氨水滴定20.0mL、0.1mol/L的盐酸,两者恰好反应,消耗20.0mL、0.1mol/L氨水,但反应生成氯化铵,氯化铵水解溶液呈酸性,所以溶液呈中性,碱应过量,故B错误;
C.NH3•H2O的电离常数Kb=$\frac{c(OH-)•c(NH4+)}{c(NH3•H2O)}$只与温度有关,随着氨水的加入,C(OH-)在增大,所以中$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)}$的值逐渐减小,故C正确;
D.当I曲线和II曲线pH均为7时,分别存在电离平衡:c(NH4+)+c(H+)=c(Cl-)+c(OH-);c(NH4+)+c(H+)=c(CH3COO-)+c(OH-),都存在:c(H+)=c(OH-),所以c(NH4+)=c(Cl-),c(NH4+)=c(CH3COO-),在盐酸中,氨水过量,在醋酸中,氨水恰好反应,所以盐酸中c(NH4+)大,则c(Cl-)>c(CH3COO-),故D错误;
故选C.
点评 本题考查酸碱混合溶液酸碱性判断及溶液中离子浓度大小比较,涉及盐类的水解、电离常数等知识,注意醋酸铵溶液呈中性,题目难度中等


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| 周 期 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 元素种类 | 2 | 8 | 8 | 18 | 18 | 32 | 32 |
| A. | 18种 | B. | 32种 | C. | 50种 | D. | 64种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
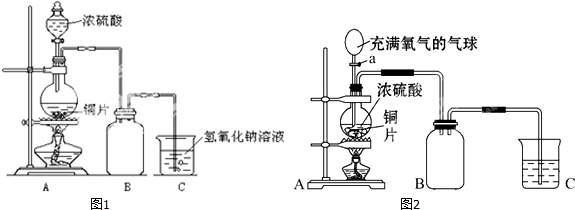
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | E(3s)>E(3p)>E(3d) | B. | E(3s)>E(2s)>E(1s) | C. | E(4f)>E(3d)>E(4s) | D. | E(5s)>E(4s)>E(4f) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
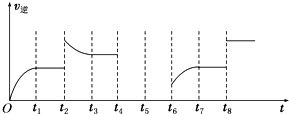 丙烷是液化石油气的主要成分,在燃烧时能放出大量的热,作为能源广泛应用于生产和日常生活中.
丙烷是液化石油气的主要成分,在燃烧时能放出大量的热,作为能源广泛应用于生产和日常生活中.| 容器 编号 | 起始时各物质 的物质的量/mol | 达到平衡 的时间/min | 达到平衡时 体系能量的 变化/kJ | |||
| CO | H2O | CO2 | H2 | |||
| A | 1.5 | 1.9 | 0 | 0 | ta | 放出热量:36.9 |
| B | 3 | 3.8 | 0 | 0 | tb | 放出热量:Q |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 合成氨反应在低温下能够自发进行,是因为反应物键能之和大于生成物键能之和 | |
| B. | 元素分析仪可以确定物质中是否含有C、H、O、N、S、Cl、Br等元素,原子吸收光谱可以确定物质中含有哪些金属元素 | |
| C. | 人们利用元素周期律在过渡元素中寻找各种性能优良的催化剂,以降低化学反应的活化能,从而起到很好的节能效果 | |
| D. | 超高分辨率荧光显微镜能够观察到纳米尺度的物质,用它可以获得蛋白质溶液中的分子图象 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
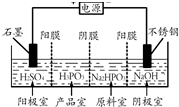 亚磷酸(H3PO3)可用作检测汞、金、银、铅、碘酸等的分析试剂.
亚磷酸(H3PO3)可用作检测汞、金、银、铅、碘酸等的分析试剂.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正丁烷和异丁烷互为同分异构体 | |
| B. | 乙醇和乙酸都能与氢氧化钠溶液反应 | |
| C. | 淀粉和蛋白质的水解产物都是氨基酸 | |
| D. | 葡萄糖和蔗糖都能发生水解反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com