
��11�֣�A��B��C��D��E��F�������������±仯��ϵ��E�ǵ���ɫ��ĩ���жϣ�
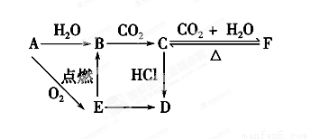
��1��д��A��B��C��D��E��F�Ļ�ѧʽ��
B.________��C.________��D.________��E��________��
��2��д���йط�Ӧ�Ļ�ѧ����ʽ(�����ӷ�Ӧ��ֱ��д���ӷ���ʽ)
E��B�� _______________��C��F�� _______________________��F��C�� ________________________��
��3������ʵ�鷽���У�����ȷ�ⶨNa2CO3��NaHCO3�������Na2CO3������������
A. ȡa�˻�����ּ��ȣ�����b��
B. ȡa�˻����������ϡ�����ַ�Ӧ�����ȡ����ɡ����գ���b�˹���
C. ȡa�˻����������ϡ�����ַ�Ӧ���ݳ�����ֱ���ü�ʯ�����գ�����b��
D. ȡa�˻����������Ba(OH)2��Һ��ַ�Ӧ�����ˡ�ϴ�ӡ���ɣ���b�˹��塣
��1�� B��NaOH C��Na2CO3 D��NaCl E��Na2O2
��2�� 2Na2O2��2H2O===4Na����4OH����O2����CO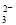 ��H2O��CO2===2HCO
��H2O��CO2===2HCO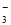
2NaHCO3 Na2CO3��H2O��CO2��
Na2CO3��H2O��CO2��
��3�� C
��������
���������A�������ڵ�ȼʱ��������ɫ��ĩ����A��Na��E��Na2O2��A��ˮ����B����B��NaOH;NaOH��Һ��ͨ��CO2�����C��Na2CO3����Na2CO3��Һ��ͨ�������CO2�����F��NaHCO3; NaHCO3���ȶ������ȷֽ����Na2CO3��Na2CO3��HCl������Ӧ����D��NaCl����1�� A��B��C��D��E��F�Ļ�ѧʽ�ֱ���B��NaOH��C��Na2CO3��D��NaCl��E��Na2O2����2�� E��B�����ӷ���ʽ��2Na2O2��2H2O===4Na����4OH����O2����C��F�����ӷ���ʽ��CO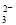 ��H2O��CO2===2HCO
��H2O��CO2===2HCO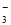 ��F��C�Ļ�ѧ����ʽ�ǣ�2NaHCO3
��F��C�Ļ�ѧ����ʽ�ǣ�2NaHCO3  Na2CO3��H2O��CO2������3��A. ȡa�˻�����ּ��ȣ�ֻ��NaHCO3��ֽ����Na2CO3��CO2��ˮ�����ص���������CO2��ˮ�������ͣ����Ը��ݼ��������b�˾Ϳ��Լ����NaHCO3����������˾���ȷ�ⶨNa2CO3��NaHCO3�������Na2CO3�������������� B. ���߶��������ᷢ����Ӧ�����õ���������NaCl.����ԭ�������Na2CO3��NaHCO3�����ʵ����ֱ���x��y,������г������飺106x+84y=a��2x+y=b��58.5��������⣬�õ�Na2CO3������������ͻ�õ�Na2CO3�������������� C. �ڻ�������������ᷢ����Ӧʱ��������CO2��ˮ���������Ա���ʯ�����գ���˲���ȷ��CO2���������Ͳ��ܼ��������и��Ե����������Բ���ȷ��Na2CO3������������ȷ��D.���߶��ܹ���Ba(OH)2������Ӧ����BaCO3����������ԭ�������Na2CO3��NaHCO3�����ʵ����ֱ���x��y,������г������飺106x+84y=a�� x+y=b��197��������⣬���Լ���õ�Na2CO3������������ͻ�õ�Na2CO3��������������
Na2CO3��H2O��CO2������3��A. ȡa�˻�����ּ��ȣ�ֻ��NaHCO3��ֽ����Na2CO3��CO2��ˮ�����ص���������CO2��ˮ�������ͣ����Ը��ݼ��������b�˾Ϳ��Լ����NaHCO3����������˾���ȷ�ⶨNa2CO3��NaHCO3�������Na2CO3�������������� B. ���߶��������ᷢ����Ӧ�����õ���������NaCl.����ԭ�������Na2CO3��NaHCO3�����ʵ����ֱ���x��y,������г������飺106x+84y=a��2x+y=b��58.5��������⣬�õ�Na2CO3������������ͻ�õ�Na2CO3�������������� C. �ڻ�������������ᷢ����Ӧʱ��������CO2��ˮ���������Ա���ʯ�����գ���˲���ȷ��CO2���������Ͳ��ܼ��������и��Ե����������Բ���ȷ��Na2CO3������������ȷ��D.���߶��ܹ���Ba(OH)2������Ӧ����BaCO3����������ԭ�������Na2CO3��NaHCO3�����ʵ����ֱ���x��y,������г������飺106x+84y=a�� x+y=b��197��������⣬���Լ���õ�Na2CO3������������ͻ�õ�Na2CO3��������������
���㣺�������ʵ��ƶϡ�����ʽ����д��������к��еijɷֺ����IJⶨ�������жϵ�֪ʶ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡ��ݸ�и�����һ�ε��п������ƻ�ѧ�Ծ��������棩 ���ͣ������
��16�֣��ߴ���ˮ�Ȼ��Ⱦ���(SrCl2��6H2O)���кܸߵľ��ü�ֵ����ҵ����������ˮ��̼���ȣ�SrCO3��Ϊԭ��(�������������Ļ������)���Ʊ��ߴ���ˮ�Ȼ��Ⱦ���Ĺ���Ϊ��
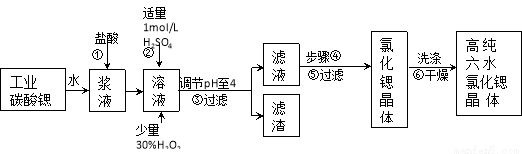
��֪�� ��. SrCl2��6H2O ������61��ʱ��ʼʧȥ�ᾧˮ��100��ʱʧȥȫ���ᾧˮ��
��.�й��������↑ʼ��������ȫ������pH����
�������� | Fe(OH)3 | Fe(OH)2 |
��ʼ������pH | 1.5 | 6.5 |
������ȫ��pH | 3.7 | 9.7 |
��1�������ټӿ췴Ӧ���ʵĴ�ʩ�� (дһ��)��̼���������ᷴӦ�����ӷ���ʽ ��
��2�����������£�����30% H2O2��Һ����Fe2+������Fe3+�������ӷ���ʽΪ ��
��3���ڲ����-�۵Ĺ����У�����Һ��pHֵ��1������4ʱ�����õ��Լ�Ϊ_______��
A����ˮ B���������ȷ�ĩ C�� �������� D��̼���ƾ���
��4����������������������Ҫ�ɷ��� (�ѧʽ)��
��5������ܵIJ����� �� ��
��6����ҵ�����ȷ紵����ˮ�Ȼ��ȣ����˵��¶��� ��
A��50~60�� B��70~80�� C��80~100�� D��100������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ������ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���й����л������������ȷ����
A��ʯ�͵ķ����ú���������Ƿ����˻�ѧ�仯
B��������ˮ�����ۻ�Ͽ��Ƴ��屽
C������һ�������¼��ܷ���ȡ����Ӧ�����ܷ����ӳɷ�Ӧ,�����ܷ���������Ӧ
D����ά�ء���֬�͵�������һ�������¶���ˮ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ������ѧ�ڵڶ����¿�������ѧ�Ծ��������棩 ���ͣ�ѡ����
���з�Ӧ�У�Ϊ���Ƶ�������������ԭ���õ�HCl���ٵ���
A��MnO2+ŨHCl B��KMnO4+HCl
C��KClO3+HCl D��������ᣨ���Ե缫��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ������ѧ�ڵڶ����¿�������ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪��Ӧ��KClO3��6HCl(Ũ)��KCl��3Cl2����3H2O���ݴ��ж�����˵����ȷ����
A����Ӧ�����ﶼ���ڵ���� B��HClȫ������������Ӧ
C���÷�Ӧ����������KClO3��Cl2ǿ D��1mol KClO3�ڷ�Ӧ�еõ�6mole��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ���и���10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���й����Ƽ��仯�����˵����ȷ����
���ƼغϽ�ͨ��״���³�Һ̬������ԭ�ӷ�Ӧ�ѵĵ��ȼ�
���ƵĻ�ѧ���ʻ��ã��������ƿɱ������л��ܼ�CCl4��
�����ڿ����л�����������ȼ����������ȼ�ո�Ϊ����
�������ƱȽϻ��ã��������ܴ�����Һ���û����������˳������ƺ���Ľ���
����������ijЩ��������������Ʊ�����
��Na2CO3��Һ�ܸ�����Һ��Ӧ�������ܸ�����Һ��Ӧ
A���٢ڢۢ� B���ڢۢ� C���٢� D����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ���и���10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
ij��ѧ��ȤС���ڿ����У���ijһ����Һ�ɷ�(��֪����������ԭ������)�����˼�⣬�������μ�������±���ʾ
������ | ��Һ�м������������ |
��һ�� | KCl��K2SO4��Na2CO3��NaCl |
�ڶ��� | KCl��AlCl3��Na2SO4��K2CO3 |
������ | Na2SO4��KCl��K2CO3��NaCl |
������˵����������
A�����μ��������ȷ
B������Һ�е����������ж�
C��Ϊ�˼���SO42-��Ӧ�ȼӹ���ϡ������ٵμ�Ba(NO3)2���۲��Ƿ��г�������
D��Ϊ��ȷ���Ƿ����CO32-�����������еμ�CaCl2��Һ���۲��Ƿ��г�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ�����и�����ѧ������������ѧ�Ծ���A���������棩 ���ͣ�ѡ����
�������ӷ���ʽ��������ʵ�������ȷ����
A��������ˮ��Ӧ��Cl2+H2O=2H++Cl��+ClO��
B����Ũ������MnO2��Ӧ��ȡ����������MnO2��2H����2Cl��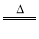 Mn2����Cl2����2H2O
Mn2����Cl2����2H2O
C����С�մ�����θ����ࣺHCO3��+H+=CO2��+H2O
D��Fe3O4��ϡHNO3��Ӧ��Fe3O4��8H+ =Fe2+��2Fe3+��4H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ�ij��и�����ѧ�ڵ�һ�ν��Բ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��4.6 g Cu��Mg��ȫ����Ũ������Һ�У���Ӧ������Ļ�ԭ����Ϊ4480mL NO2����336 mL N2O4����(��״����)����Ӧ�����Һ�У��������NaOH��Һ�����ɳ���������Ϊ ( )
A��9.02 g B��8.51 g C��8.26 g D��7.04 g
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com