

(1)在抗击“禽流感”斗争中,消毒液需求量猛增。利用如右图装置制备消毒液:电解氯化钠溶液制取“84”消毒液,氯气被完全吸收,则对电极名称和消毒液的主要成分判断正确的是( )
A.a为正极,b为负极;NaClO和NaCl B.a为负极,b为正极;NaClO和NaCl
C.a为阳极,b为阴极;HClO和NaCl D.a为阴极,b为阳极;HClO和NaCl
(2)适当改变电极也可用上图装置制取氢氧化亚铁。通电后,溶液中产生大量白色沉淀,且较长时间不变色。下列说法中正确的是( )
A.电源中的a一定为正极,b一定为负极
B.不能使用氯化钠溶液作电解液
C.A、B两端都必须使用铁作电极
D.B电极发生的反应可能是:2H2O+2e-![]() H2↑+2OH-
H2↑+2OH-
解析:本题考查根据电化学原理设计创新实验能力。(1)题眼是“氯气被完全吸收”,“环保型”。该题可根据题干提供的要求,通过读图判断直流电源如何连接才能达到制得消毒液的目的。上端的电极如果接通电源正极,通电电解时,产生氯气,氯气由玻璃管直接排放到大气中,污染环境。如果电源的正极接通下方的电极,下端产生氯气,上端产生氢气和氢氧化钠,氢气由玻璃管直接排出,氯气在向上运动的过程中,被氢氧化钠溶液吸收后,生成次氯酸钠和氯化钠溶液。
(2)制取氢氧化亚铁,必须提供OH-、Fe2+;根据电解原理,与电源负极相接的电极为电解池的阴极,与电源正极相连的电极为阳极。阴极:物质得到电子,发生还原反应;阳极:物质失去电子,发生氧化反应。所以,铁必须为阳极,发生Fe-2e-![]() Fe2+。要在阴极得到电子发生还原反应,只有发生2H2O+2e-
Fe2+。要在阴极得到电子发生还原反应,只有发生2H2O+2e-![]() 2OH-+H2↑,电解质溶液增强导电性,但不参与阴极反应,即金属活泼性顺序表中氢前的金属盐溶液或强碱溶液符合条件。不能用酸作电解质溶液,因为电解酸溶液,开始不能产生OH-,无氢氧化亚铁生成。综上所述,电源的电极不确定,可以用氯化钠溶液作电解液,阳极必须用铁作电极,阴极不一定用铁作电极,可以用其他电极;b电极可能是阴极,发生还原反应:2H2O+2e-
2OH-+H2↑,电解质溶液增强导电性,但不参与阴极反应,即金属活泼性顺序表中氢前的金属盐溶液或强碱溶液符合条件。不能用酸作电解质溶液,因为电解酸溶液,开始不能产生OH-,无氢氧化亚铁生成。综上所述,电源的电极不确定,可以用氯化钠溶液作电解液,阳极必须用铁作电极,阴极不一定用铁作电极,可以用其他电极;b电极可能是阴极,发生还原反应:2H2O+2e-![]() H2↑+2OH-。D项,重在“可能”二字。氢气从导管逸出,可以在A极产生,也可以在B极产生。
H2↑+2OH-。D项,重在“可能”二字。氢气从导管逸出,可以在A极产生,也可以在B极产生。
答案:(1)B (2)D


科目:高中化学 来源: 题型:阅读理解
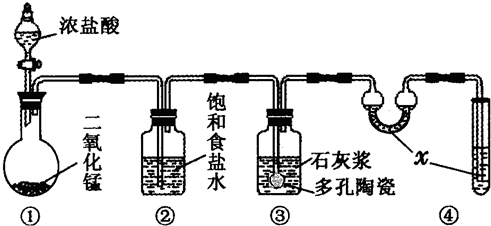
| 滴定次数 | 1 | 2 | 3 |
| KI溶液体积/mL | 19.98 | 20.02 | 20.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| △ |
| △ |

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
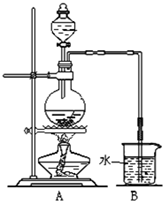 如图是某研究性学习小组利用实验室制氯气的装置设计制取氯水并进行相关实验.
如图是某研究性学习小组利用实验室制氯气的装置设计制取氯水并进行相关实验.
| ||
| ||
 )
) )
)查看答案和解析>>
科目:高中化学 来源: 题型:

| 1 |
| 2 |
| 1 |
| 2 |
| ||
. |
查看答案和解析>>
科目:高中化学 来源: 题型:
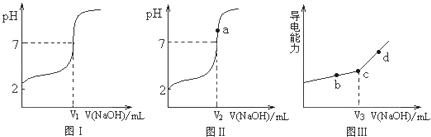
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com