
有a、b、c、d、f五种前四周期元素,原子序数依次增大,a、b、c三种元素的基态原子具有相同的能层和能级,第一电离能I1(a)<I1(c)<I1(b)且其中基态b原子的2p轨道处半充满状态,已知bc2+与ac2互为等电子体,d为周期表前四周期中电负性最小的元素,f的原子序数为29。请回答下列问题。(如需表示具体元素请用相应的元素符号)
(1)写出bc2+的电子式__________,基态f原子的核外电子排布式为___________。
(2)b的简单氢化物极易溶于c的简单氢化物,其主要原因是???????????????? 。

(3)化合物甲由c、d两种元素组成,其晶胞如甲图,甲的化学式___________。
(4)化合物乙的部分结构如乙图,乙由a、b两元素组成,硬度超过金刚石。①乙的晶体类型为________________________,其硬度超过金刚石的原因是_________________________。
②乙的晶体中a、b两种元素原子的杂化方式均为___________________。
(1)[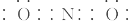 ]+?????? 1s22s22p63s23p63d104s1
]+?????? 1s22s22p63s23p63d104s1
(2)两种氢化物都是极性分子,分子间都能形成氢键????? (3)KO2??????
(4)①原子晶体? C—N键的键长小于C—C键,C—N键的键能大于C—C键?? ②sp3杂化
【解析】
试题分析:基态b原子的2p轨道处半充满状态,则b原子的电子排布为1s22s22p3,b元素为N元素,a、b、c三种元素的基态原子具有相同的能层和能级,第一电离能I1(a)<I1(c)<I1(b),bc2+与ac2互为等电子体,说明b原子电子数比a原子数多1个,则a为C元素,c为O元素,d为周期表前四周期中电负性最小的元素,则d为K元素,f的原子序数为29,则f为Cu元素。
(1)bc2+为NO2+,与ac2即CO2 互为等电子体,所以N原子分别与O原子形成双键,所以bc2+电子式为:[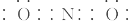 ]+;Cu原子核外电子数为29,所以核外电子排布式为:1s22s22p63s23p63d104s1
]+;Cu原子核外电子数为29,所以核外电子排布式为:1s22s22p63s23p63d104s1
(2)b的简单氢化物极易溶于c的简单氢化物,即NH3极易溶于H2O,是因为NH3与H2O都是极性分子,分子间都能形成氢键。
(3)根据甲的晶胞示意图可以看出K位于8个顶点和6个面的面心,所以1个晶胞含K:8×1/8+6×1/2=4,两个O原子形成的原子团位于晶胞的12个棱的中心和体心,则数目为:12×1/4+1=4,所以甲的化学式为:KO2
(4)①因为乙的硬度超过金刚石,所以乙的晶体类型为原子晶体;乙是由C、N两元素组成,晶体内共价键为C—N键,金刚石内共价键为C—C键,因为C—N键的键长小于C—C键,C—N键的键能大于C—C键,所以硬度超过金刚石。
②因为乙晶体结构类似金刚石,C、N原子都形成4个共价键,所以C、N原子的杂化方式均为sp3杂化。
考点:本题考查元素的推断、电子排布、溶解性的判断、晶体结构与性质的分析、原子杂化方式。


 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:


| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:058
有A、B、C、D、F、G七瓶不同物质的溶液,它们分别是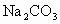 、
、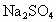 、KCl、
、KCl、 、
、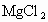 、
、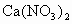 和
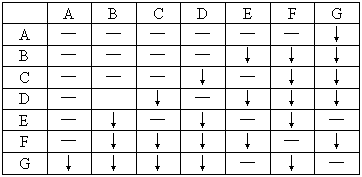
和 溶液中的一种.为了鉴别,各取少量溶液进行两两混合,实验结果如表所示.表中“↓”表示生成沉淀或微溶化合物,“—”表示观察不到明显变化.试回答下列问题.
溶液中的一种.为了鉴别,各取少量溶液进行两两混合,实验结果如表所示.表中“↓”表示生成沉淀或微溶化合物,“—”表示观察不到明显变化.试回答下列问题.
(1)A的化学式是_________,G的化学式是_________.判断理由是______________.
(2)写出其余几种物质的化学式.B:______________,C:_______,D:_______,E:______________,F:_________________.
查看答案和解析>>
科目:高中化学 来源: 题型:022
有A、B、C、D、F、G七瓶不同物质的溶液,它们分别是 、
、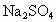 、KCl、
、KCl、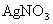 、
、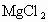 、
、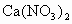 和
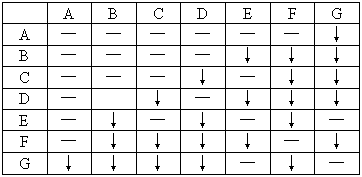
和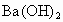 溶液中的一种.为了鉴别,各取少量溶液进行两两混合,实验结果如表所示.表中“↓”表示生成沉淀或微溶化合物,“—”表示观察不到明显变化.试回答下列问题.
溶液中的一种.为了鉴别,各取少量溶液进行两两混合,实验结果如表所示.表中“↓”表示生成沉淀或微溶化合物,“—”表示观察不到明显变化.试回答下列问题.
(1)A的化学式是_________,G的化学式是_________.判断理由是______________.
(2)写出其余几种物质的化学式.B:______________,C:_______,D:_______,E:______________,F:_________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com