
| A. | 1mol | B. | 1.5mol | C. | 2mol | D. | 2.5mol |
分析 硫酸虽然是稀溶液,但是和硝酸混合在一起,为硝酸和铜反应提供氢离子,使生成物中的硝酸根离子继续与氢离子相遇,形成硝酸,仍然和铜反应,利用铜与硝酸反应的离子方程式中及铜和氢离子的比例来进行计算.
解答 解:混合溶液中n(H+)=4mol+1mol×2=6mol,n(Cu)=3mol,n(NO3-)=4mol,
由3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O可知,
3molCu反应需要消耗8molH+,2molNO3-,则H+不足,H+完全反应,
设生成NO的物质的量为x,则
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
8 2
6mol x
$\frac{8}{6}=\frac{2}{x}$,解得x=1.5mol,
故选B.
点评 本题考查硝酸及硝酸盐的性质,明确发生的离子反应及氢离子不足是解答本题的关键,学生容易直接利用硝酸的物质的量计算而出错.


科目:高中化学 来源: 题型:解答题
 蛋白质中含有C、H、O、N、S等元素,食物中的铁主要以三价铁与蛋白质和羧酸结合成络合物的形式存在.
蛋白质中含有C、H、O、N、S等元素,食物中的铁主要以三价铁与蛋白质和羧酸结合成络合物的形式存在.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 铁片为正极,碳棒为负极 | |
| B. | 碳棒附近的溶液可使酚酞变红 | |
| C. | 铁被腐蚀,碳棒上有氯气放出 | |
| D. | 导线上有电流通过,电流方向是由铁极流向碳极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数:a>b>c>d | B. | 离子半径:A(n+1)+>Bn+>C(n+1)->Dn- | ||
| C. | 原子半径:A>B>C>D | D. | 单质还原性:B>A,单质氧化性:D>C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | a和d是同分异构体 | B. | b和c是同系物 | ||
| C. | 可以用酸性高锰酸钾溶液区分a和c | D. | 只有b和c能发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
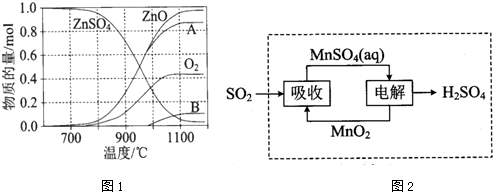
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
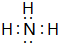 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某有机物同系物组成可用通式CnH2n+2表示 | |
| B. | 同系物互为同分异构体 | |
| C. | 两个同系物之间相对分子质量相差14或14的整数倍 | |
| D. | 同系物具有相似的化学性质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com