
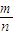 知,混合气体的平均摩尔质量是34g/mol,利用十字交叉法确定两种物质的物质的量,再根据N=nNA、m=nM、
知,混合气体的平均摩尔质量是34g/mol,利用十字交叉法确定两种物质的物质的量,再根据N=nNA、m=nM、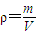 确定正误.
确定正误.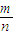 知,混合气体的平均摩尔质量是34g/mol,利用十字交叉法确定两种物质的物质的量之比
知,混合气体的平均摩尔质量是34g/mol,利用十字交叉法确定两种物质的物质的量之比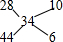 ,所以一氧化碳和二氧化碳的物质的量之比=10:6=5:3,则n(CO)=
,所以一氧化碳和二氧化碳的物质的量之比=10:6=5:3,则n(CO)= mol,n(CO2)=
mol,n(CO2)= mol,
mol,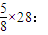
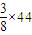 =35:33,故正确;
=35:33,故正确;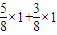 ):(
):(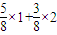 )=8:11,故正确;
)=8:11,故正确;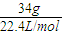 =1.52g/L,故正确;
=1.52g/L,故正确;

 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.只有① | B.只有② | C.①和④ | D.①②③④都正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com