
氯化钠是海水的主要成分,也是人类生活中不能缺少的一种物质。下列关于氯化钠的说法正确的是
A.氯化钠溶液能导电,所以氯化钠溶液是电解质
B.氯化钠溶液可杀菌,说明氯化钠溶液具有强氧化性
C.电解熔融氯化钠和电解氯化钠溶液的产物相同
D.加碘食盐是指添加了碘的化合物的氯化钠
科目:高中化学 来源:2016届山东省高三上10月阶段质检化学试卷(解析版) 题型:选择题
用惰性电极电解一定量的硫酸铜溶液,实验装置如图甲,电解过程中的实验数据如图乙。横坐标表示转移电子的物质的量,纵坐标表示产生气体的总体积(标准状况)。则下列说法不正确的是

A.电解过程中,a电极表面先有红色物质析出,后有气泡产生
B.b电极上发生的反应方程式为:4OH--4e- = 2H2O+O2↑
C.从开始到Q点时收集到的混合气体的平均摩尔质量为12 g/ mol
D.从开始到P点收集到的气体是O2
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高三上学期10月调考理综化学试卷(解析版) 题型:填空题
【化学——选修3:物质结构与性质】(15分)
(1)按已知的原子结构规律,27号元素在周期表中的位置是 ,其价电子的轨道排布图为 。
(2)若en代表乙二胺( 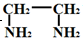 ),则配合物[Pt(en)2]Cl4中心离子的配位原子数为 。
),则配合物[Pt(en)2]Cl4中心离子的配位原子数为 。
(3)BeCl2是共价分子,可以以单体、二聚体和多聚体形式存在。它们的结构简式如下,指出Be的杂化轨道类型。
① 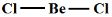 ②
② 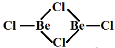
③ 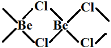
(4)磷化硼(BP)是一种有价值的耐磨硬涂层材料,这种陶瓷材料可作为金属表面的保护薄膜。它是通过在高温氢气氛围下(>750℃)三溴化硼和三溴化磷反应制得。BP晶胞如图所示。
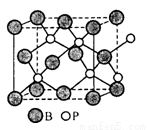
①画出三溴化硼和三溴化磷的空间结构式。
三溴化硼
三溴化磷
②在BP晶胞中B的堆积方式为 。
③计算当晶胞晶格参数为478pm(即图中立方体的每条边长为478pm)时磷化硼中硼原子和磷原子之间的最近距离 。
查看答案和解析>>
科目:高中化学 来源:2016届福建省莆田市高三上学期第一次月考化学试卷(解析版) 题型:实验题
附加题(16分)某学生对SO2与漂粉精的反应进行实验探究:
操作 | 现象 |
取4 g漂粉精固体,加入100 mL水 | 部分固体溶解,溶液略有颜色 |
过滤,测漂粉精溶液的pH | pH试纸先变蓝(约为12),后褪色 |
| i.ii.稍后,出现浑浊,溶液变为黄绿色; iii.稍后,产生大量白色沉淀,黄绿色褪去 液面上方出现白雾; |
(1)Cl2和Ca(OH)2制取漂粉精的化学方程式是__________________________。
(2)pH试纸颜色的变化说明漂粉精溶液具有的性质是____________________。
(3)向水中持续通入SO2,未观察到白雾。推测现象i的白雾由HCl小液滴形成。进行如下实验:
a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用酸化的AgNO3溶液检验白雾,产生白色沉淀。
① 实验a的目的是__________________________。
②由实验a、b不能判断白雾中含有HCl,理由是________________________
(4)现象ii中溶液变为黄绿色的可能原因:随溶液酸性的增强,漂粉精的有效成分和Cl-发生反应。通过进一步实验确认了这种可能性,其实验方案是_________________________
(5)将A瓶中混合物过滤、洗涤,得到沉淀X
①向沉淀X中加入稀HCl,无明显变化。取上层清液,加入BaCl2溶液,产生白色沉淀。则沉淀X中含有的物质是____________________
②用离子方程式解释现象iii中黄绿色褪去的原因:_________________ ____________
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三上学期第二次检测化学试卷(解析版) 题型:推断题
【有机化学基础】高分子化合物G 是制备某种特种复合材料的基体。合成G 的一种路线如下:
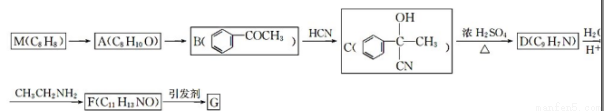
已知下列信息:
①G 的结构简式为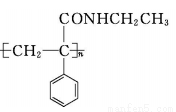
②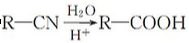
③羟基直接与碳碳双键相连的结构不稳定:
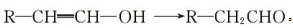
请回答下列问题:
(1)M 的化学名称为 ,D 的结构简式为 ,E 中含氧官能团的名称为 。
(2)B 生成C 的反应类型是 ,F 生成G 的反应类型是 。
(3)由M 生成A 的化学方程式为 。
(4)只含苯环一个环状结构且遇FeCl3 溶液不显紫色的B 的同分异构体有 种(不包括B,不考虑立体异构),其中核磁共振氢谱为四组峰,且峰面积之比为3∶2∶2∶1 的同分异构体的结构简式为 。
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三上学期第一次月考化学试卷(解析版) 题型:选择题
在一定条件下,某化合物X受热分【解析】
2X=A↑+2B↑+4C↑
测得反应后生成的混合气体对H2的相对密度为11.43,相同条件下,X的相对分子质量是
A.11.43 B.22.85 C.80.01 D.160.02
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁实验中学高一上10月阶段测化学试卷(解析版) 题型:选择题
a g NH3含b个氢原子,则阿伏加德罗常数可表示为
A.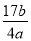 B.
B.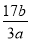 C.
C.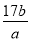 D.
D.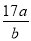
查看答案和解析>>
科目:高中化学 来源:2016届江西省南昌市高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列关于物质性质或检验的叙述正确的是
A.在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+
B.气体通过湿润的蓝色石蕊试纸,试纸变红,证明原气体中含有氨气
C.用铂丝灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,可能有K+
D.将气体通入澄清石灰水,溶液变浑浊,证明原气体是CO2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上第一次月考化学试卷(解析版) 题型:填空题
某温度(T ℃)下的溶液中,c(H+)=10-x mol·L-1,c(OH-)=10-y mol·L-1,x与y的关系如图所示,请回答下列问题:
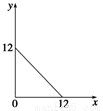
(1)此温度下,水的离子积Kw为______________,则该温度T_____________25(填“>”、“< 或“=”)。
(2)在此温度下,向Ba(OH)2溶液中逐滴加入pH=a的盐酸,测得混合溶液的部分pH如表所示。
实验序号 | Ba(OH)2溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
① | 22.00 | 0.00 | 8 |
② | 22.00 | 18.00 | 7 |
③ | 22.00 | 22.00 | 6 |
假设溶液混合前后的体积变化忽略不计,则a=_____________________,实验②中由水电离产生的c(OH-)=________________mol·L-1。
(3)在此温度下,将0.1 mol·L-1的NaHSO4溶液与0.1 mol·L-1的Ba(OH)2溶液按下表中甲、乙、丙、丁不同方式混合:
甲 | 乙 | 丙 | 丁 | |
0.1 mol·L-1 Ba(OH)2溶液体积/mL | 10 | 10 | 10 | 10 |
0.1 mol·L-1 NaHSO4溶液体积/mL | 5 | 10 | 15 | 20 |
①按丁方式混合后,所得溶液显________________(填“酸”、“碱”或“中”)性。
②写出按乙方式混合后,反应的离子方程式:_________________________。
③按甲方式混合后,所得溶液的pH为______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com