
下列说法中正确的是( )
A.凡是放热反应都是自发的,凡是吸热反应都是非自发的
B.自发反应熵一定增大,非自发反应熵一定减小或不变
C.要判断反应进行的方向,必须综合考虑体系的焓变和熵变
D.自发反应在任何条件下都能实现
科目:高中化学 来源: 题型:
把1.12 升(标准状况下)HCl气体溶于水,配制成250 mL的溶液,计算:
(1)该溶液中HCl的物质的量浓度。
(2)若将该溶液与足量的锌反应,在标准状况下能生成氢气多少升?
查看答案和解析>>
科目:高中化学 来源: 题型:
为了有效除去工业食盐中的Ca2+、Mg2+、SO42—,加入试剂的合理顺序为
A.NaOH—Na2CO3—BaCl2 B.NaOH—BaCl2—Na2CO3
C.BaCl2—NaOH—Na2CO3 D.Na2CO3—BaCl2—NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
下列热化学方程式正确的是(注:△H的绝对值均正确)
A.C2H5OH(l)+3O2(g)==2CO2(g) +3H2O(g) △H= -1367.0 kJ/mol(燃烧热)
B.NaOH(aq) + HCl(aq) == NaCl(aq) + H2O(l) △H= - 57.3kJ/mol(中和热)
C.S(s) + O2(g) == SO2(g) △H= -269.8kJ/mol(反应热)
D.2NO2==O2+2NO △H= +116.2kJ/mol(反应热)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于平衡常数K的说法中,正确的是( )
A.在任何条件下,化学平衡常数是一个恒定值
B.改变反应物浓度或生成物浓度都会改变平衡常数K
C.平衡常数K只与温度有关,与反应浓度、压强无关
D.从平衡常数K的大小不能推断一个反应进行的程度
查看答案和解析>>
科目:高中化学 来源: 题型:
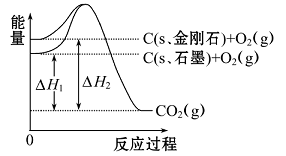
如图所示,ΔH1=-393.5 kJ·mol-1,ΔH2=-395.4 kJ·mol-1,下列说法或表示式正确的是( )
A.C(s、石墨)====C(s、金刚石)ΔH=+1.9 kJ·mol-1
B.石墨和金刚石的转化是物理变化
C.金刚石的稳定性强于石墨
D.1 mol石墨的能量比1 mol金刚石的总能量大
查看答案和解析>>
科目:高中化学 来源: 题型:
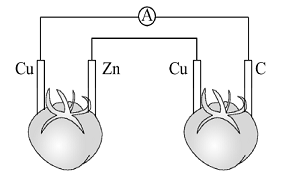
如图所示,铜片、锌片和石墨棒用导线连接后插入番茄里,电流计中有电流通过,则下列说法正确的是( )
A.锌片是负极
B.两个铜片上都发生氧化反应
C.石墨是阴极
D.两个番茄都形成原电池
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学用语正确的是
A.氯化钠的电子式: 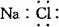
B.乙烯的结构简式:C2H4
C.硅的原子结构示意图: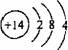
D.硫酸的电离方程式:Na2SO4=Na2++SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于同分异构体判断正确的是( )
A.分子式为C8H10的芳香烃有3个,分别为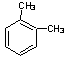 、
、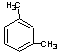 和
和 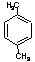
B.分子式为C2H6O的同分异构体有两个,分别是 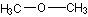 和 CH3CH2OH
和 CH3CH2OH
C.分子式为C4H8的烯烃同分异构体有2个,分别为CH2=CHCH2CH3、CH3CH=CHCH3
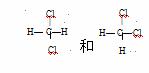
D. 是两种不同的物质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com