
【题目】化学与生活、科技关系密切。下列有关叙述正确的是
a.液氨可作制冷剂是因为其气化时可放出大量的热
B.将青蒿在乙醚中浸取,通过分馏可提取治疗疟疾的青蒿素
C.钢制品、铝制品在日常生活中被广泛应用是因为铁、铝为活泼金属
D.久置的漂白粉变质是因为漂白粉与空气中的O2反应
科目:高中化学 来源: 题型:
【题目】如下图所示,a、b是石墨电极,通电一段时间后,b极附近溶液显红色。下列说法正确的是
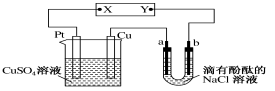
A.X极是电源负极,Y极是电源正极
B.Cu电极上增重6.4 g时,b极产生1.12 L(标准状况)气体
C.电解过程中CuSO4溶液的pH逐渐增大
D.a极的电极反应式为2Cl--2e-=Cl2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列两个气态物质之间的反应:C2H2(g)+H2(g)![]() C2H4(g) ①
C2H4(g) ①
2CH4(g)![]() C2H4(g)+2H2(g) ②
C2H4(g)+2H2(g) ②
已知在降低温度时①式平衡向右移动,②式平衡向左移动,则下列三个反应:(Q1、Q2、Q3均为正值)
C(s)+2H2(g)=CH4(g) ΔH=-Q1 I
2C(s)+H2(g)=C2H2(g) ΔH=-Q2 II
2C(s)+2H2(g)=C2H4(g) ΔH=-Q3 III
Q值大小比较正确的是
A.Q1>Q3>Q2 B.Q1>Q2>Q3 C.Q2>Q1>Q3 D.Q3>Q1>Q2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下,回答下列问题:
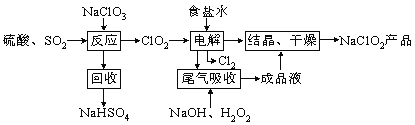
(1)ClO2的沸点为283K,纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下更安全。写出“反应”步骤中生成ClO2的化学方程式 。
(2)“尾气吸收”是吸收“电解”过程排出的少量ClO2。
①在尾气吸收过程中,可代替H2O2的试剂是 (填序号)。
A.Na2O2 B.Na2S C.FeCl2 D.KMnO4
②提高尾气的吸收效率的可行措施有 (填序号)。
A.尾气吸收时充分搅拌吸收液 B.适当加快尾气的通入速率
C.将温度控制在20℃以下 D.加水稀释尾气吸收液
③此吸收反应中,氧化剂与还原剂的物质的量之比为 。
(3)在碱性溶液中NaClO2比较稳定,在酸性溶液中,ClO2-和H+结合为HClO2,HClO2是唯一的亚卤酸,不稳定,易分解产生Cl2、ClO2和H2O,写出HClO2分解的化学方程式: 。
(4)已知NaClO2的溶解度随温度升高而增大,NaClO2饱和溶液在38℃以上60℃以下会析出NaClO2,在NaClO2析出过程中可能混有的杂质是 (填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用浓度为0.1000mol·L-1的NaOH溶液分别逐滴加入到20.00mL 0.1000mol·L-1的HX、HY溶液中,pH随NaOH溶液体积的变化如图。下列说法正确 ( )
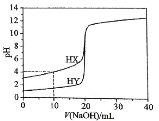
A.V(NaOH)=10.00 mL时,c(X-)>c(Na+)>c(H+)>c(OH-)
B.V(NaOH)=20.00 mL时,两份溶液中,c(X-)>c(Y-)
C.V(NaOH)=20.00 mL时,c(Na+) > c(X-) >c(OH-)>c(H+)
D.pH=7时,两份溶液中,c(X-)=c(Y-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 100 ℃纯水的pH=6,所以水在100 ℃时呈酸性
B. pH=3的盐酸溶液,稀释至10倍后pH>4
C. 0.2 mol·L-1的醋酸,与等体积水混合后pH=1
D. 常温时,pH=3的盐酸与pH=11的氢氧化钠等体积混合后pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题.

(1)该浓盐酸中HCl的物质的量浓度为 ______ molL-1.
(2)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是______ .
A.溶液中HCl的物质的量
B.溶液的浓度
C.溶液中Cl-的数目
D.溶液的密度
(3)配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次并在操作步骤空白处填上适当仪器名称) ______ .
A.用30mL水洗涤 ______ 2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用 ______ 加水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1~2cm处
(4)在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在括 号内填“偏大”,“偏小”,或“无影响”)
a.用量筒量取浓盐酸时俯视观察凹液面 ______
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水 ______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,某反应达到平衡,平衡常数K = c(CO)c(H2O)/c(CO2)c(H2),恒容时,温度升高,H2浓度减小。下列说法正确的是
A.该反应的焓变为正值
B.恒温恒容下,增大压强,H2浓度一定减小
C.升高温度,逆反应速率减小
D.该反应的化学方程式为CO+H2O ![]() CO2+H2
CO2+H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com