
发展“碳一化学”,开发利用我国相对丰富的煤炭资源具有重要的战略意义和经济价值。下面是以焦炭为原料,经“碳一化学”途径制取乙二醇的过程:

(1)该过程中产生的的CO可继续与水蒸气发生可逆反应得到CO2和H2,此反应的平衡常数表达式K =____________。
(2)CH3OH(l)气化时吸收的热量为27 kJ/mol,CH3OH(g)的燃烧热为677 kJ/mol,请写出CH3OH(l)完全燃烧的热化学方程式_________________。
(3) “催化还原”反应制乙二醇原理如下:
CH3OOC-COOCH3(g)+4H2(g)
 HOCH2-CH2OH(g)+2CH3OH(g)
△H = -34 kJ/mol
HOCH2-CH2OH(g)+2CH3OH(g)
△H = -34 kJ/mol
为探究实际生产的最佳条件,某科研小组进行了多方面研究。下图表示乙二醇达到平衡时的产率随原料投料比[n(氢气)/n(草酸二甲酯)]和压强的变化关系,其中三条曲线分别表示体系压强为1.5 MPa、2.5 MPa、3.5 MPa的情况,则曲线甲对应的压强是P(甲)=___________。

(4)草酸二甲酯水解产物草酸(H2C2O4)为二元中强酸
① 草酸氢钾溶液中存在如下平衡:
H2O H++OH-、HC2O4-
H++OH-、HC2O4- H++C2O42-和
。
H++C2O42-和
。
② 向0.1 mol/L的草酸氢钾溶液里滴加NaOH溶液至中性,此时溶液里各粒子浓度关系正确的是 (填序号)。
a.c(K+) = c(HC2O4-) + c(H2C2O4) + c(C2O42-)
b.c(K+) + c(Na+) = c(HC2O4-) + c(C2O42-)
c.c(Na+) = c(H2C2O4) + c(C2O42-)
d.c(K+) > c(Na+)
(5)以甲醇为原料,使用酸性电解质构成燃料电池,该燃料电池的负极反应式为 ;若以甲烷代替该燃料电池中的甲醇,向外界提供相等电量,则每代替32 g甲醇,所需标准状况下的甲烷的体积为 L。
(14分)
(1)K=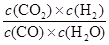
(2)CH3OH(l) +3/2O2(g) = CO2(g)+2H2O(l) ∆H = -650 kJ /mol
(3)3.5 MPa
(4)①
HC2O4-+H2O H2C2O4+OH- ② a d
H2C2O4+OH- ② a d
(5)CH3OH+H2O-6e-=CO2+6H+ 16.8
【解析】
试题分析:
(2)① CH3OH(l)= CH3OH(g) ∆H = 27 kJ /mol
② CH3OH(g)+3/2 O2(g)=CO2(g)+2H2O(g) ∆H = -677 kJ /mol
①+② 得 CH3OH(l) +3/2O2(g) = CO2(g)+2H2O(l) ∆H = -650 kJ /mol
(3)压强越大,速率越大,达平衡所需的时间越短,甲的时间最短,对应的压强最大,为3.5 MPa
(4)①HC2O4- 既有电离又有水解。②a为物料守恒,正确;b为电荷守恒,错误,正确的为c(H+)+c(K+) + c(Na+) = c(HC2O4-) + 2c(C2O42-)+c(OH-);c错误;向0.1 mol/L的草酸氢钾溶液里滴加NaOH溶液至中性,草酸氢钾溶液呈酸性,若草酸氢钾和NaOH溶液恰好反应,生成K2C2O4和Na2C2O4,它们水解呈碱性,要呈中性,应是草酸氢钾>NaOH,即c(K+) > c(Na+),d正确,选a d 。
(5)总: CH3OH+3/2O2= CO2+2H2O 酸性电解质的正极反应式:3/2O2+6 H++6e-=3 H2O
负极反应式=总-正极反应式 得:CH3OH+H2O-6e-=CO2+6H+
CH4 +2H2O -8e-= CO2+8 H+ ,32 g甲醇相当于1mol ,有6 mol电子转移,提供相等电量,需3/4 mol CH4,V=nVm=3/4*22.4= 16.8(L)
考点:本题考查平衡常数,盖斯定律,平衡移动,溶液里的离子平衡,溶液里的离子浓度比较,原电池的电极反应等知识。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:江苏省扬州中学2012届高三上学期12月练习化学试题 题型:022
能源危机是当前全球问题,开源节流是应对能源危机的重要举措.
(1)下列做法有助于能源“开源节流”的是________(填字母).
a.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
b.大力开采煤、石油和天然气以满足人们日益增长的能源需求
c.开发太阳能、水能、风能、地热等新能源、减少使用煤、石油等化石燃料
d.减少资源消耗,增加资源的重复使用、资源的循环再生
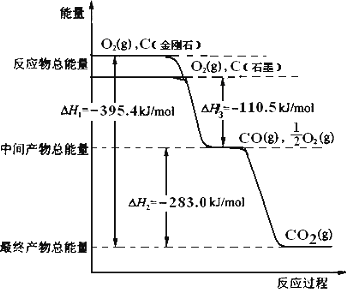
(2)金刚石和石墨均为碳的同素异形体,它们燃烧氧气不足时生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如图所示.
(a)
在通常状况下,金刚石和石墨中________(填“金刚石”或“石墨”)更稳定,石墨的燃烧热为________kJ·mol-1.(b)12 g
石墨在一定量空气中燃烧,生成气体36 g,该过程放出的热量________kJ.(3)已知:N2(g)+O2(g)![]() 2NO(g);ΔH=+180.0 kJ·mol-1
2NO(g);ΔH=+180.0 kJ·mol-1
综合上述有关信息,请写出CO除NO的热化学方程式________.
美国斯坦福大学研究人员最近发明一种“水”电池,这种电池能利用淡水与海水之间含盐量的差别进行发电.
(4)研究表明,电池的正极用二氧化锰纳米棒为材料可提高发电效率,这是利用纳米材料具有________特性,能与钠离子充分接触.
(5)海水中的“水”电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,该电池负极反应式为________;当生成1 mol Na2Mn5O10转移________mol电子.
查看答案和解析>>
科目:高中化学 来源: 题型:
(16分) 能源危机是当前全球问题,开源节流是应对能源危机的重要举措。
⑴下列做法有助于能源“开源节流”的是 ▲ (填字母)。
a.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
b.大力开采煤、石油和天然气以满足人们日益增长的能源需求
c.开发太阳能、水能、风能、地热等新能源、减少使用煤、石油等化石燃料
d.减少资源消耗,增加资源的重复使用、资源的循环再生
(2)金刚石和石墨均为碳的同素异形体,它们燃烧氧气不足时生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如右图所示。
(a)在通常状况下,金刚石和石墨中____▲___(填“金刚石”或“石墨”)更稳定,石墨的燃烧热为____▲___ kJ·mol-1。
(b)12 g石墨在一定量空气中燃烧,生成气体36g,该过程放出的热量 ▲ kJ。
(3)已知:N2(g)+O2(g)=2NO(g);ΔH=+180.0 kJ·mol-1。
综合上述有关信息,请写出CO除NO的热化学方程式 ▲ 。
美国斯坦福大学研究人员最近发明一种“水”电池,这种电池能利用淡水与海水之间含盐量的差别进行发电。
(4)研究表明,电池的正极用二氧化锰纳米棒为材料可提高发电效率,这是利用纳米材料具有
▲ 特性,能与钠离子充分接触。
(5)海水中的“水”电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,该电池负极反应式为 ▲ ;当生成1 mol Na2Mn5O10转移 ▲ mol电子。
查看答案和解析>>
科目:高中化学 来源:2012届江苏省扬州中学高三12月练习测试化学试卷 题型:填空题
(16分)能源危机是当前全球问题,开源节流是应对能源危机的重要举措。
⑴下列做法有助于能源“开源节流”的是 ▲ (填字母)。
a.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
b.大力开采煤、石油和天然气以满足人们日益增长的能源需求
c.开发太阳能、水能、风能、地热等新能源、减少使用煤、石油等化石燃料
d.减少资源消耗,增加资源的重复使用、资源的循环再生
(2)金刚石和石墨均为碳的同素异形体,它们燃烧氧气不足时生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如右图所示。 
(a)在通常状况下,金刚石和石墨中____▲___(填“金刚石”或“石墨”)更稳定,石墨的燃烧热为____▲___ kJ·mol-1。
(b)12 g石墨在一定量空气中燃烧,生成气体36g,该过程放出的热量 ▲ kJ。
(3)已知:N2(g)+O2(g)=2NO(g);ΔH=+180.0 kJ·mol-1。
综合上述有关信息,请写出CO除NO的热化学方程式 ▲ 。
美国斯坦福大学研究人员最近发明一种“水”电池,这种电池能利用淡水与海水之间含盐量的差别进行发电。
(4)研究表明,电池的正极用二氧化锰纳米棒为材料可提高发电效率,这是利用纳米材料具有
▲ 特性,能与钠离子充分接触。
(5)海水中的“水”电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,该电池负极反应式为 ▲ ;当生成1 mol Na2Mn5O10转移 ▲ mol电子。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江苏省高三12月练习测试化学试卷 题型:填空题
(16分) 能源危机是当前全球问题,开源节流是应对能源危机的重要举措。
⑴下列做法有助于能源“开源节流”的是 ▲ (填字母)。
a.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
b.大力开采煤、石油和天然气以满足人们日益增长的能源需求
c.开发太阳能、水能、风能、地热等新能源、减少使用煤、石油等化石燃料
d.减少资源消耗,增加资源的重复使用、资源的循环再生
(2)金刚石和石墨均为碳的同素异形体,它们燃烧氧气不足时生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如右图所示。

(a)在通常状况下,金刚石和石墨中____▲___(填“金刚石”或“石墨”)更稳定,石墨的燃烧热为____▲___ kJ·mol-1。
(b)12 g石墨在一定量空气中燃烧,生成气体36g,该过程放出的热量 ▲ kJ。
(3)已知:N2(g)+O2(g)=2NO(g);ΔH=+180.0 kJ·mol-1。
综合上述有关信息,请写出CO除NO的热化学方程式 ▲ 。
美国斯坦福大学研究人员最近发明一种“水”电池,这种电池能利用淡水与海水之间含盐量的差别进行发电。
(4)研究表明,电池的正极用二氧化锰纳米棒为材料可提高发电效率,这是利用纳米材料具有
▲ 特性,能与钠离子充分接触。
(5)海水中的“水”电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,该电池负极反应式为 ▲ ;当生成1 mol Na2Mn5O10转移 ▲ mol电子。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
I.(4分)低碳经济、节能减排、应对气候变暖已成为全人类发展共同面临的课题。
(1)现在人们使用乙醇汽油作为汽车燃料充分体现了低碳经济,物质的量相同的乙醇与汽油(设为C8H18)均完全燃烧后产生的CO2的物质的量之比为 ;人们已尝试使用 作为汽车燃料可真正实现“二氧化碳零排放"。
(2)汽车尾气催化转化器能将汽车尾气中的CO和NOx反应生成可参与大气生态环境循环的无毒的两 种气体,写出CO和NOx在一定条件下反应的化学方程式: 。
(3)用可降解的“玉米塑料”替代一次性饭盒或制作证件封面和胸卡,目的是防止产生 污染。
Ⅱ.(5分)下列是生活常用的物质:
A.碳酸氢钠 &青霉素 C葡萄糖D.苯甲酸钠 E.柠檬黄
可用作食品着色剂的是 (填字母,下同);可直接进入血液补充能量的是 ;可用作食品防腐剂的是 ;属于抗生素的是 ;治疗胃酸过多的是 。
Ⅲ.(6分)材料是人类赖以生存和发展的重要物质基础。
(1)晶体硅常用于半导体材料,二氧化硅是光纤的主要成分,晶体硅和二氧化硅都属于 晶体。(填“离子”“分子”或“原子”)
(2)三大合成材料是指:合成纤维、 、 。
(3)金属是一种重要的材料,人类的生活和生产都离不开金属。
①工业炼铁的主要化学反应方程式为 。
②炒过菜的铁锅未及时洗净易腐蚀出现红褐色锈斑,它是铁锅在潮湿的空气中发生 腐蚀造成的,铁锅锈蚀的负极反应方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com