
| A、乙酸的结构简式:C2H4O2 |
| B、中子数为20的氯原子:1720Cl |
C、F-的结构示意图: |
D、NH4Br的电子式: |
 ,故C正确;
,故C正确;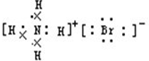 ,故D错误;
,故D错误;

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
 A、B、C三种短周期元素在周期表中的位置如图所示,已知A、C可分别与B形成化合物X和Y,A与B的质子数之和等于C的质子数,则下列说法正确的组合是( )
A、B、C三种短周期元素在周期表中的位置如图所示,已知A、C可分别与B形成化合物X和Y,A与B的质子数之和等于C的质子数,则下列说法正确的组合是( )| A、①②③④ | B、②④ |
| C、①② | D、①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝箔在空气中受热熔化,并不滴落,说明铝与氧气没有发生化学反应 |
| B、硅在电子工业中是最重要的半导体材料,广泛用于制作光导纤维 |
| C、二氧化硫是一种有毒气体,所以不能用于杀菌消毒 |
| D、氨很容易液化,液氨气化吸收大量的热,所以液氨常用作制冷剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入少量W,逆反应速率增大,平衡向左移动 |
| B、增大压强,正反应速率增大,逆反应速率减小 |
| C、温度、体积不变,充入He气增大压强,反应速率会加快 |
| D、升高温度,混合气体的平均相对分子质量减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 短周期元素Q、R、T、W在元素周期表中的位置如图,其中T所处的周期序数与主族序数相等,下列叙述正确的是( )
短周期元素Q、R、T、W在元素周期表中的位置如图,其中T所处的周期序数与主族序数相等,下列叙述正确的是( )| A、离子半径:Tm+>Wn- |
| B、非金属性:Q<W |
| C、R的氢化物的水溶液呈酸性 |
| D、Q的氧化物都是酸性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是周期表中短周期的一部分,W、X、Y三种元素原子核外电子数之和等于X的质量数,X原子核内质子数和中子数相等.下列叙述中不正确的是( )
如图是周期表中短周期的一部分,W、X、Y三种元素原子核外电子数之和等于X的质量数,X原子核内质子数和中子数相等.下列叙述中不正确的是( )| A、三种元素的原子半径的大小顺序是W<Y<X |
| B、X元素的氧化物、氢化物的水溶液都呈酸性 |
| C、Y元素的单质是非金属单质中唯一能跟水发生激烈反应的单质 |
| D、W最高价氧化物对应水化物具有强酸性,气态氢化物的水溶液具有弱碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、仅③ | B、①③ | C、②④ | D、②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素周期表中第一纵行的元素都是碱金属 |
| B、元素的性质随着原子序数的递增而呈周期性变化 |
| C、随着元素原子序数的递增,元素的最高正价从+1到+7,负价从-7到-1重复出现 |
| D、利用周期律,可以在金属与非金属的交界处找到催化剂、耐高温和耐腐蚀的合金材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 短周期元素X、Y、W、Q在元素周期表中的相对位置如图所示.Y是地壳中含量最多的元素.下列说法正确的是( )
短周期元素X、Y、W、Q在元素周期表中的相对位置如图所示.Y是地壳中含量最多的元素.下列说法正确的是( )| A、1mol Q单质与氢氧化钠溶液反应转移的电子数目为2NA |
| B、X的气态氢化物能使湿润的蓝色石蕊试纸变红 |
| C、氢化物的沸点:H2Y>HQ |
| D、最髙价氧化物的水化物的酸性:W>Q |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com