
��ͼ��ʾװ�ó�ȥ��CN-��Cl-��ˮ�е�CN-ʱ��������ҺpHΪ9~10������������ClO-��CN-����Ϊ��������Ⱦ�����壬����˵����ȷ���ǣ� ��
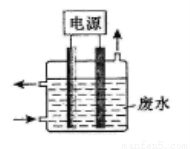
A��������ʯī����������������
B�������ĵ缫��ӦʽΪ��2CN-+12OH-��10e-=N2��+2CO32-+6H2O
C�������ĵ缫��ӦʽΪ�� Cl-+2OH- +2e-=ClO-+H2O
D����ȥCN-�ķ�Ӧ��2CN-+5ClO-+2H+=N2��+2CO2��+5Cl-+H2O

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ�߶��϶������Ի�ѧ�Ծ��������棩 ���ͣ������
��1����0.2mol/L HA ��Һ�� 0.1mol/L NaOH��Һ�������ϣ���û����Һ��c(Na+)>c(A?)����(�á�>������<����=����д���пհ�)���ٻ����Һ��c(A?)______c(HA)���ڻ����Һ��c(HA)+c(A?)______0.1mol?L?1��
��2������ʱ��ȡ0.1mol•L-1 HX��Һ��0.1mol•L-1 NaOH��Һ�������ϣ���Ϻ���Һ����ı仯���ƣ�����û����Һ��pH=8���Իش��������⣺
�ٻ����Һ����ˮ�������c(OH-)��0.1mol•L-1 NaOH��Һ����ˮ�������c(OH-)֮��Ϊ______��
����֪NH4X��Һ�����ԣ���֪��HX��Һ���뵽Na2CO3��Һ��������ų������ƶ�(NH4)2CO3��Һ��pH______7��ѡ���������������=������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���㽭�����и�����ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
�������ʵ���Ϊ4mol��Na2O2��Al2(SO4)3�����Ͷ������ˮ�У���ַ�Ӧ������ymol������y��0��������x��ʾԭ�������Na2O2�����ʵ������Խ���y=f(x)�ĺ�����ϵʽ����x��ȡֵ��y=f(x)��ϵʽ��д�ڱ��ڣ���������Ҳ�ɲ������䣩��������ͼ�л�������ͼ��

xֵ | y=f(x) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��������Ϫ��һ��ѧ������ѧ�����п�������ѧ�Ծ��������棩 ���ͣ��ƶ���
�����������A��B��Ϊͬ���칹�壬����C��H��O����Ԫ�ء����Ҹ��л�����������ת����ϵ��
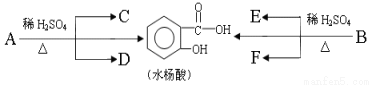
����C�ܷ���������Ӧ��C�����ɿ�ѧ���������϶��õ���F����������������C��C��D����Է���������ͬ�IJ�ͬ���л��
��1��C�����������ŵ������� ��
��2��A�ķ���ʽ�� ��B�Ľṹ��ʽ�� ��
��3����ȫȼ��ʱ��1 mol D��1 mol ���� �ĺ�������ͬ������ĸ���ţ���
a��C3H6O3 b��C3H8O c��C2H4 d��C2H6O2
��4��C��F��Ӧ�Ļ�ѧ����ʽ�� ����Ӧ������____________��
��5��ˮ����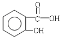 ��ͬ���칹��ܶ࣬д�����к��������������������ͬ���칹��Ľṹ��ʽ�� ��
��ͬ���칹��ܶ࣬д�����к��������������������ͬ���칹��Ľṹ��ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�찲��ʡ�����ϵ��Ĵζο���ѧ�Ծ��������棩 ���ͣ�ѡ����
Fe3+��Fe2+��NO3-��NH4+��H+��H2O����������һ��������ԭ��Ӧ�еķ�Ӧ���������.���������в���ȷ����( )
A����ԭ����ΪNH4+
B���������뻹ԭ�������ʵ���֮��Ϊ1:8
C��Fe3+��Fe2+�ֱ����ڷ�Ӧ���������
D�����Ѹ÷�Ӧ���Ϊԭ���,����ӦΪFe2+-e-=Fe3+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�켪�ֳ��������ѧУ�����ϵ�һ���ʼ컯ѧ�Ծ��������棩 ���ͣ�ѡ����
���л�ѧʵ����ʵ������ͻ���۶���ȷ����
A���ò�����պȡ������ˮ������pH��ֽ�ϣ�Ȼ�����ɫ�����գ��ɲⶨ������ˮ��pH
B����10mL 0��1 mol/L��AgNO3��Һ�еμ�10��0��1 mol/L��NaCl��Һ���а�ɫ�������ɣ��������еμ�0��1 mol/L��KI��Һ��������Ϊ��ɫ��˵����ͬ�¶���AgCl�ܽ�ȴ���AgI���ܽ��
C����1 mL 1%��NaOH��Һ�м���2 mL 2%��CuSO4��Һ�����ټ���0��5 mL�л���Y�����ȣ�δ����ש��ɫ������˵��Y�в���ȩ��
D��ȡ����±����Y�ڼ�����Һ��ˮ�⣬�������ữ�����ԣ��ٵμ�AgNO3��Һ�����ɵ���ɫ������˵��±�����к�����Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�츣��ʡ������ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��ȷ����
A�������ʵ���Ũ�ȵ�FeBr2��CuCl2�Ļ��Һ�ö��Ե缫������������Cu2++2Br-=Cu��+Br2
B��H218O��Ͷ��Na2O2��2H218O+2Na2O2=4Na++4OH-+��O2��
C����������Һ����μ���Ba(OH)2��Һ��SO42-ǡ�ó�����ȫ��
2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3��+3BaSO4��
D��Fe(NO3)3��������Һ��ͨ���������⣺2Fe3++H2S=2Fe2++S��+2H+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������������������ѧ��һ��10�»�ѧ���������棩 ���ͣ�ѡ����
���Ʊ�ˮ��;���Ƶ��۵�ϵ�;������ˮ��ӦʱҪ�ų�����;������ˮ��Ӧ����Һ�ʼ���.ijѧ����һС�������Ͷ����з�̪��Һ��ˮ��,��ʵ����֤�������ĵ������е�
A���٢� B���٢ڢ� C���٢ۢ� D���٢ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�������ʡ������ѧ��12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��pH��l������ƽ���ֳ�2�ݣ�l�ݼ�����ˮ����1�ݼ�������������ʵ���Ũ����ͬ������NaOH��Һ��pH��������1��������ˮ��NaOH��Һ�������Ϊ: �� ��
A. 9 B.10 C.11 D.12
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com