(2011?晋中模拟)某强酸性溶液X中含有Ba
2+、Al
3+、NH
4+、Fe
2+、Fe
3+、CO
32-、SO
32-、SO
42-、Cl
-、NO
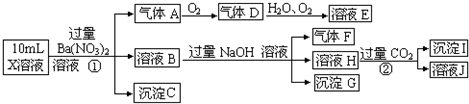
3-中的一种或几种,取该溶液进行连续实验,实验内容如下:
根据以上信息,回答下列问题:
(1)上述离子中,溶液X中除H
+外还肯定含有的离子是
Al3+、NH4+、Fe2+、SO42-
Al3+、NH4+、Fe2+、SO42-
,不能确定是否含有的离子(Q)是
Fe3+、Cl-
Fe3+、Cl-
,若要确定该Q(若不止一种,可任选一种)不存在,其最可靠的化学方法是:
取少量X溶液放在试管中,加入几滴KSCN,溶液不变红色说明无Fe3+;或者取少量B溶液放在试管中,加入几滴AgNO3溶液,无白色沉淀说明无Cl-
取少量X溶液放在试管中,加入几滴KSCN,溶液不变红色说明无Fe3+;或者取少量B溶液放在试管中,加入几滴AgNO3溶液,无白色沉淀说明无Cl-
.
(2)沉淀G的化学式为
Fe(OH)3
Fe(OH)3
.
(3)写出有关离子方程式:
①中生成A:
3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O
3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O
.
②:
CO2+OH-=HCO3-,AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
CO2+OH-=HCO3-,AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
.
(4)假设测定A、F、I均为0.01mol,10mL X溶液中n(H
+)=0.04mol,且不能确定含有的离子(Q)只有一种.当沉淀C物质的量
>0.07mol
>0.07mol
,表明Q离子一定是
Fe3+
Fe3+
.




 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案