
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | 熔点℃ | 沸点℃ | 密度 g?cm-3 | 溶解性 |
| 乙二醇( C2H6O2) | -11.5 | 198 | 1.11 | 易溶于水 和乙醇 |
| 丙三醇(C3H8O3) | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
Ⅰ.如图是中学化学中常用于混合物的分离与提纯的装置,请根据装置回答问题: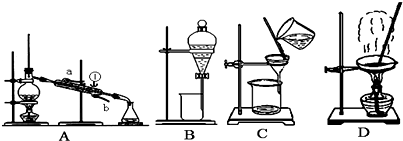
(1)从氯化钾溶液中得到氯化钾固体,选择装置______(填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置______.
(2)从碘水中分离出I2,选择装置______,该分离方法的名称为______.
(3)装置A中①的名称是______,进出水的方向是______.
(4)装置B在分液时为使液体顺利下滴,应进行的具体操作是______.(填代表选项的字母)
A.应该先将分液漏斗上的活塞拿下后再打开旋塞放出液体
B.加热
C.使分液漏斗上的活塞上的凹槽对准分液漏斗上的小孔后再打开旋塞放出液体.
Ⅱ.某同学按下列步骤配制250mL 0.2mol?L-1 NaCl溶液,请回答有关问题.
| 实验步骤 | 有关问题 |
| ①计算所需NaCl的质量 | |
| ②称量NaCl固体 | 用托盘天平需要称量NaCl的质量为______g. |
| ③将NaCl加入100mL烧杯中,并加入适量水 | 为了加快溶解速率,可以采取哪些措施:______. |
| ④将烧杯中溶液转移至250mL容量瓶中 | 为了防止溶液溅出,应采取什么措施:______. |
| ⑤向容量瓶中加蒸馏水至刻度线 | 在进行此操作时当加水至刻度线1-2厘米处应如何操作: ______. |
(1)配制时,实验室提供了以下仪器:烧杯、100mL量筒、玻璃棒、托盘天平(带砝码)、胶头滴管,还缺少的玻璃仪器是______.上述实验中使用容量瓶前应______.
(2)取出该NaCl溶液10mL加水稀释到100mL,稀释后溶液中Na+的物质的量浓度是______.
(3)若进行⑤步操作时加蒸馏水超过刻度线,则需______.
(4)配制NaCl溶液时,下列操作情况会使结果偏高的是______.
A.移液前,容量瓶中有少量蒸馏水
B.溶解搅拌时有液体飞溅
C.定容时俯视容量瓶瓶颈刻度线
D.定容后,倒置容量瓶摇匀经平放静置,液面低于刻度线,再加水定容.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com