
 [CuCl4]2- +4H2O
[CuCl4]2- +4H2O科目:高中化学 来源:不详 题型:计算题
 2Z + W;正反应为放热反应,(四物质均为气体)。达到平衡时。VA="1.2a" L,试回答: (A在的活塞可移动)
2Z + W;正反应为放热反应,(四物质均为气体)。达到平衡时。VA="1.2a" L,试回答: (A在的活塞可移动) 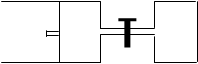
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 温度/℃ | 25 | t1 | t2 |
| 水的离子积常数 | 1×10-14 | a | 1×10-12 |
 5Ca2+(aq)+3PO(aq)+OH-(aq);Ksp=2.5×10-59。进食后,细菌和酶作用于食物,产生有机酸,这时牙齿就会受到腐蚀,其原因是 。
5Ca2+(aq)+3PO(aq)+OH-(aq);Ksp=2.5×10-59。进食后,细菌和酶作用于食物,产生有机酸,这时牙齿就会受到腐蚀,其原因是 。 N2O4(g)的平衡常数K= 。若NO2起始浓度为2 mol/L ,相同条件下,NO2的最大转化率为 。
N2O4(g)的平衡常数K= 。若NO2起始浓度为2 mol/L ,相同条件下,NO2的最大转化率为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2SO3(g),达到平衡时, 18O存在于( )
2SO3(g),达到平衡时, 18O存在于( )| A.只存在于O 2中 |
| B.只存在于O 2和SO3中 |
| C.只存在于SO2和SO3中 |
| D.SO3、SO2和O 2中都有可能存在 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
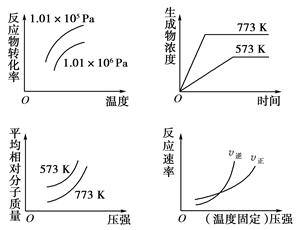
A.N2(g)+3H2(g) 2NH3(g)ΔH=-Q1 kJ/mol(Q1>0) 2NH3(g)ΔH=-Q1 kJ/mol(Q1>0) |
B.H2(g)+CO(g) C(s)+H2O(g)ΔH=+Q4 kJ/mol(Q4>0) C(s)+H2O(g)ΔH=+Q4 kJ/mol(Q4>0) |
C.4NH3(g)+5O2(g) 4NO(g)+6H2O(g)ΔH=-Q3 kJ/mol(Q3>0) 4NO(g)+6H2O(g)ΔH=-Q3 kJ/mol(Q3>0) |
D.2SO3(g)? 2SO2(g)+O2(g)ΔH=+Q2 kJ/mol(Q2>0) 2SO2(g)+O2(g)ΔH=+Q2 kJ/mol(Q2>0) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
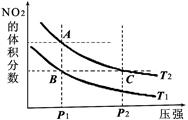
 N2O4(g)。如下图1所示,烧瓶A、B中装有相同浓度的NO2和N2O4的混合气体,中间用止水夹K夹紧,烧杯甲、乙分别盛放100mL冷水和热水。
N2O4(g)。如下图1所示,烧瓶A、B中装有相同浓度的NO2和N2O4的混合气体,中间用止水夹K夹紧,烧杯甲、乙分别盛放100mL冷水和热水。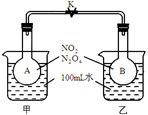
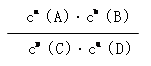
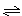 pC(g)+qD(g)中K=
pC(g)+qD(g)中K= 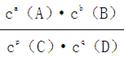
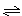 2NH3(g)的平衡常数表示式K=
2NH3(g)的平衡常数表示式K=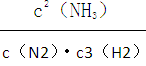
 N2O4(g)的平衡常数表达式K=
N2O4(g)的平衡常数表达式K= 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 C(g)+2D(g);ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是( )
C(g)+2D(g);ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是( )| A.①② | B.④ | C.③ | D.④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
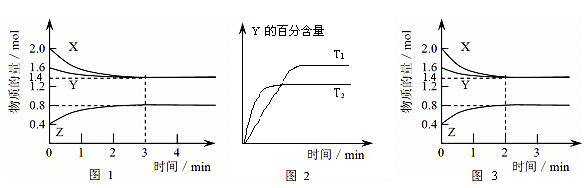
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
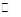 2C(g),现等物质的量的投料反应物A、B于恒温恒容体系I和恒温、恒压体系II中,达平衡时体系I中A的物质的量浓度为M,体系II中A的物质的量浓度为m,则M与m的关系为
2C(g),现等物质的量的投料反应物A、B于恒温恒容体系I和恒温、恒压体系II中,达平衡时体系I中A的物质的量浓度为M,体系II中A的物质的量浓度为m,则M与m的关系为查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com