


 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 目前流通的第五套人民币硬币材料分别为:1元硬币为铜芯镀镍合金,5角硬币为铜芯镀铜合金,1角硬币为硬铝合金.请回答:(题目中的百分含量均为质量分数)
目前流通的第五套人民币硬币材料分别为:1元硬币为铜芯镀镍合金,5角硬币为铜芯镀铜合金,1角硬币为硬铝合金.请回答:(题目中的百分含量均为质量分数)| 电极 | a | b | c | d | e | f |
| 石墨 | 石墨 | 铜 | 钢 | 钢 | 铜 | |
| 溶液 | NaCl溶液 | CuSO4溶液 | CuSO4溶液 | |||
查看答案和解析>>
科目:高中化学 来源: 题型:
目前流通的第五套人民币硬币材料分别为:1元硬币为铜芯镀镍合金,5角硬币为铜芯镀铜合金,1角硬币为硬铝合金。请回答:(题目中的百分含量均为质量分数)
(1)钢是含碳量为0.03%~2%的___________(填物质类别名称)。
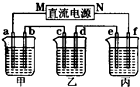
(2)下图所示的装置中,甲、乙、丙三个烧杯分别盛放足量的溶液,电极及溶液如下表所示:
| 电极 | a | b | c | d | e | f |
| 石墨 | 石墨 | 铜 | 钢 | 钢 | 铜 | |
| 溶液 | NaCl溶液 | CuSO4溶液 | CuSO4溶液 |
通电后电极a上可产生能使湿润的碘化钾淀粉试纸变蓝的气体。
①上述装置中M极为直流电源的_________极(填“正”或“负”),电极b上发生的电极反应式为__________________________________________。
②若在钢币上镀铜,应选择_______烧杯(填“乙”或“丙”),当电极a上生成标准状况下气体2240 mL时,理论上可在电极_______(填字母)上镀铜_______g。
(3)工业上以铝土矿(主要成分Al2O3·nH2O,含少量的氧化铁和石英等杂质)为原料生产铝。为除去铝土矿样品中氧化铁和石英杂质,要将粉碎、筛选后的铝土矿样品溶解在足量的氢氧化钠溶液中处理,请写出有关反应的离子方程式__________________________。
(4)已知硬铝中含Cu:2.2%~5%、Mg:0.2%~3%、Mn:0.3%~1.5%、Si:0.5%,其余是Al。1角硬币单枚质量为2.20克,若想制得1角硬币1百万枚,理论上至少需要含Al2O3 90%的铝土矿约_______吨(小数点后保留一位数字)。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年重庆市高三第六次月考(理综)化学部分 题型:填空题
目前流通的第五套人民币硬币材料分别为:1元硬币为铜芯镀镍合金,5角硬币为铜芯镀铜合金,1角硬币为硬铝合金。请回答:(题目中的百分含量均为质量分数)
(1)钢是含碳量为0.03%~2%的___________(填物质类别名称)。
(2)下图所示的装置中,甲、乙、丙三个烧杯分别盛放足量的溶液,电极及溶液如下表所示:

|
电极 |
a[来源:ZXXK] |
b |
c |
d |
e |
f[来源:学+科+网Z+X+X+K] |
|
石墨 |
石墨 |
铜 |
钢 |
钢 |
铜 |
|
|
溶液 |
NaCl溶液 |
CuSO4溶液 |
CuSO4溶液 |
通电后电极a上可产生能使湿润的碘化钾淀粉试纸变蓝的气体。
①上述装置中M极为直流电源的_________极(填“正”或“负”),电极b上发生的电极反应式为__________________________________________。
②若在钢币上镀铜,应选择_______烧杯(填“乙”或“丙”),当电极a上生成标准状况下气体2240 mL时,理论上可在电极_______(填字母)上镀铜_______g。
(3)工业上以铝土矿(主要成分Al2O3·nH2O,含少量的氧化铁和石英等杂质)为原料生产铝。为除去铝土矿样品中氧化铁和石英杂质,要将粉碎、筛选后的铝土矿样品溶解在足量的氢氧化钠溶液中处理,请写出有关反应的离子方程式__________________________。
(4)已知硬铝中含Cu:2.2%~5%、Mg:0.2%~3%、Mn:0.3%~1.5%、Si:0.5%,其余是Al。1角硬币单枚质量为2.20克,若想制得1角硬币1百万枚,理论上至少需要含Al2O3 90%的铝土矿约_______吨(小数点后保留一位数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com