
【题目】一种“固定CO2”的电化学装置如图。该电化学装置放电时可将CO2转化为C和Li2CO3,充电时仅使Li2CO3发生氧化反应释放出CO2和O2,下列说法正确的是
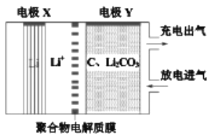
A.放电时,Li+向电极X方向移动
B.放电时,每转移4 mol e-,理论上生成 1 mol C
C.充电时,阳极反应:C+2Li2CO3-4e-=3CO2↑+4Li+
D.充电时,电极Y与外接直流电源的负极相连
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:
【题目】重铬酸钠晶体 ![]() 俗称红矾钠,在工业方面有广泛用途.我国目前主要是以铬铁矿
俗称红矾钠,在工业方面有广泛用途.我国目前主要是以铬铁矿![]() 主要成份为
主要成份为![]() ,还含有
,还含有![]() 、MgO、
、MgO、![]() 等杂质
等杂质![]() 为主要原料进行生产,其主要工艺流程如下:
为主要原料进行生产,其主要工艺流程如下:
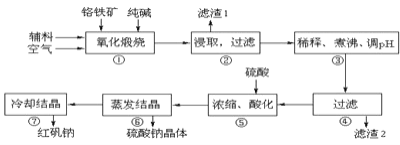
①中涉及的主要反应有:
主反应:![]()
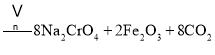
副反应: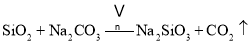 、
、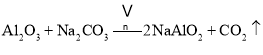
部分阳离子以氢氧化物形式完全沉淀时溶液的pH:
沉淀物 |
|
|
|
|
完全沉淀时溶液pH |
|
|
|
|
试回答下列问题:
![]() “①”
“①”
![]() “③”中调节pH至
“③”中调节pH至![]() ,目的是 ______ .
,目的是 ______ .
![]() “⑤”中加硫酸酸化的目的是使
“⑤”中加硫酸酸化的目的是使![]() 转化为
转化为![]() ,请写出该平衡转化的离子方程式: ______ .
,请写出该平衡转化的离子方程式: ______ .
![]() 称取重铬酸钠试样
称取重铬酸钠试样![]() 配成250mL溶液,取出
配成250mL溶液,取出![]() 于碘量瓶中,加入10mL
于碘量瓶中,加入10mL![]() 和足量碘化钠
和足量碘化钠![]() 铬的还原产物为
铬的还原产物为![]() ,放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用
,放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用![]() 标准溶液滴定
标准溶液滴定![]()
①判断达到滴定终点的依据是: ______ ;
②若实验中共用去![]() 标准溶液
标准溶液![]() ,所得产品的中重铬酸钠晶体的纯度
,所得产品的中重铬酸钠晶体的纯度![]() 设整个过程中其它杂质不参与反应
设整个过程中其它杂质不参与反应![]() ______ .
______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】知识的梳理和感悟是有效学习的方法之一。山大附中高二化学兴趣小组将有关“电解饱和食盐水”的相关内容进行梳理,形成如下问题(所有电极均为石墨)。电解所用的氯化钠溶液需精制,除去有影响的Ca2+、Mg2+、NH4+、SO42﹣及泥沙,其精制流程如下:
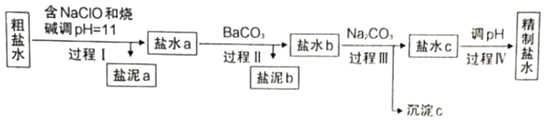
已知:①Ca2+、Mg2+开始形成相应氢氧化物沉淀的pH如表。
Ca(OH)2 | Mg(OH)2 | |
pH | ≥11.5 | ≥9.2 |
②Ksp(BaSO4)=1.1×10﹣10,Ksp(BaCO3)=2.6×10﹣9,Ksp(CaCO3)=5.0×10﹣9
(1)盐泥a除泥沙外,还含有___________(填化学式)。
(2)过程I中,NaClO的作用是将NH4+转化为N2,反应的离子方程式为________________。
(3)过程Ⅲ中,沉淀c主要成分的化学式为_____。
(4)过程Ⅳ调pH目的是除去___________(填离子符号)
(5)利用图1装置电解精制氯化钠一段时间后,气球b中的气体是_____(填化学式)
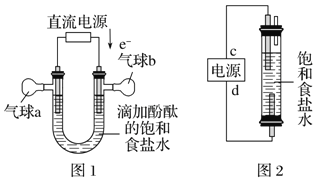
(6)利用图2制作一种环保型消毒液发生器,电解可制备“84”消毒液的有效成分NaClO,则c为电源的_____极;该发生器中反应的总离子方程式为_______________。
(7)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。如图是目前已开发出用电解法制取ClO2的新工艺。
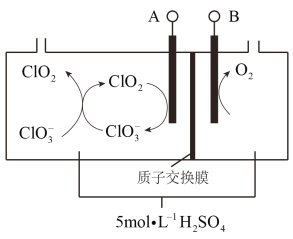
①阴极发生的反应有:_______________、__________________________。
②当阳极产生标准状况下112 mL气体时,通过阳离子交换膜离子的物质的量为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向10 mL 0.1 mol·L-lNaCl溶液和10 mL 0.1 mol·L-lK2CrO4溶液中分别滴加0.1 mol·L-lAgNO3溶液。滴加过程中pM[-lgc(Cl-)或-lgc(CrO42-)]与所加AgNO3溶液体积之间的关系如下图所示。已知Ag2CrO4为红棕色沉淀。下列说法错误的是
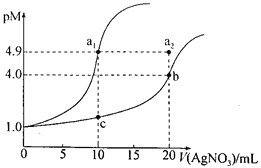
A. 该温度下,Ksp(Ag2CrO4)=4×10-12
B. al、b、c三点所示溶液中c(Ag+):al>b>c
C. 若将上述NaCl溶液浓度改为0.2mol·L-1,则a1点会平移至a2点
D. 用AgNO3标准溶液滴定NaCl溶液时,可用K2CrO4溶液作指示剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种钌(Ru)基配合物光敏染料敏化太阳能电池的原理及电池中发生的主要反应如图所示。下列说法正确的是

A. 镀铂导电玻璃的作用是传递I-
B. 电池工作时,光能转变为电能,X为电池的正极
C. 电池的电解质溶液中I-和I3-的浓度均不断减小
D. 电解质溶液中发生反应2Ru3++3I-═2Ru2++I3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种将燃料电池与电解池组合制备KMnO4的装置如图所示(电极甲、乙、丙、丁均为惰性电极)。该装置工作时,下列说法不正确的是

A. 电极丁的反应式为MnO42- -e-= MnO4-
B. 电极乙附近溶液的pH减小
C. KOH溶液的质量分数:c%>a%>b%
D. 导线中流过2 mol电子时,理论上有2molK+移入阴极区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究金属腐蚀和防腐的原理很有现实意义.

(1)甲图为人教版教材中探究钢铁的吸氧腐蚀的装置,某兴趣小组按装置试验,导管中液柱的上升缓慢,为更快更清晰地观察到液柱上升的现象,下列措施错误的________(填序号)
A.用纯氧气代替试管内空气
B.用酒精灯加热试管提高温度
C.将铁钉换成铁粉和炭粉混合粉末
D.换成更细的导管,水中滴加红墨水
(2)为探究铁钉腐蚀实验a、b两点所发生的反应,张老师进行以下实验,证明铁发生电化学腐蚀。请完成表格空白:
实验操作 | 实验现象 | 实验结论 |
ⅰ.向NaCl溶液中滴加2~3滴酚酞指示剂 | a点附近溶液出现红色 | a点电极反应为_______________ |
ⅱ.然后再滴加2~3滴铁氰化钾溶液 | b点周围出现蓝色沉淀 | b点电极反应为_______________ 沉淀的化学式为______________ |
(3)孔老师认为仅通过b中现象不能证明铁发生了电化学腐蚀,补充进行下列实验,在实验几分钟后的记录如下:
实验 | 滴管 | 现象 |
1.0 mol·L-1NaCl溶液 | 0.5 molL﹣1K3[Fe(CN)6]溶液 | 铁片表面产生大量蓝色沉淀 |
以上实验表明,K3[Fe(CN)6]具有________性
(4)赵老师设计下面装置研究弱酸性环境中腐蚀的主要形式,测定锥形瓶内气压和空气中氧气的体积分数随时间变化见图,从图中可分析,t1~t2之间主要发生_________腐蚀(填吸氧或析氢)
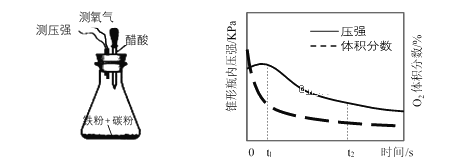
(5)金属阳极钝化形成保护膜是一种电化学防腐方法,将Fe作阳极置于H2SO4溶液中,一定条件下Fe表面形成致密Fe3O4氧化膜,试写出该阳极电极反应式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】经研究发现白蚁信息素有:![]() (2,4-二甲基-1-庚烯),
(2,4-二甲基-1-庚烯),![]() (3,7-二甲基-1-辛烯),家蚕的性信息素为:CH3(CH2)3CH=CH—CH=CH(CH2)3CH3。下列说法正确的是( )
(3,7-二甲基-1-辛烯),家蚕的性信息素为:CH3(CH2)3CH=CH—CH=CH(CH2)3CH3。下列说法正确的是( )
A.以上三种信息素互为同分异构体
B.以上三种信息素均能使溴的四氯化碳溶液褪色
C.2,4-二甲基-1-庚烯与3,7-二甲基-1-辛烯互为同系物
D.家蚕的性信息素与1molBr2加成产物只有一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨反应为 N2(g)+3H2(g) ![]() 2NH3(g)△H=+92.4kJmol﹣1,下列说法正确的是( )
2NH3(g)△H=+92.4kJmol﹣1,下列说法正确的是( )
A.一定条件下,当N2的生成速率与N2的分解速率相等时,该反应处于平衡状态
B.取1mol N2和3mol H2放在密闭容器内反应达平衡时,生成2 mol NH3
C.一定条件下反应达到平衡,再充入N2,则正反应速率增大,逆反应速率减小
D.一定条件下反应达到平衡,若升高温度,反应速率增大,平衡向正反应方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com