
|
 (提示:4FeS2+11O2
(提示:4FeS2+11O2 2Fe2O3+8SO2)
2Fe2O3+8SO2) 2Fe2O3+8SO2,可推得D是Fe2O3,A,是SO2, B是SO3, C是H2SO3。I和D发生铝热反应生成Fe和Al2O3,由纵观前面的反应,可推得G是Fe,H是Al2O3。则M的溶液为Fe(NO3)3溶液,M和C反应生成NO和Fe2(SO4)3,可得F是Fe2(SO4)3,E是Fe(OH)3。因此(1)题组成单质Fe的元素就位于第四周期Ⅷ族。(2)题反应⑦Fe和Al2O3发生铝热反应,氧化剂Al2O3与还原剂Fe的物质的量之比为1:2。(3)题②是SO2和O2反应生成SO3,是化合反应但同时也是氧化还原反应,③是SO3和水反应生成H2SO3既属于化合反应又属于非氧化还原反应,⑥是分解Fe(OH)3生成Fe2O3属于分解
2Fe2O3+8SO2,可推得D是Fe2O3,A,是SO2, B是SO3, C是H2SO3。I和D发生铝热反应生成Fe和Al2O3,由纵观前面的反应,可推得G是Fe,H是Al2O3。则M的溶液为Fe(NO3)3溶液,M和C反应生成NO和Fe2(SO4)3,可得F是Fe2(SO4)3,E是Fe(OH)3。因此(1)题组成单质Fe的元素就位于第四周期Ⅷ族。(2)题反应⑦Fe和Al2O3发生铝热反应,氧化剂Al2O3与还原剂Fe的物质的量之比为1:2。(3)题②是SO2和O2反应生成SO3,是化合反应但同时也是氧化还原反应,③是SO3和水反应生成H2SO3既属于化合反应又属于非氧化还原反应,⑥是分解Fe(OH)3生成Fe2O3属于分解

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| A.在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素 |
| B.原子最外层电子数相同的元素不一定在同一族 |
| C.ⅧA族所含元素种类最多 |
| D.元素周期表是元素周期律的具体表现形式 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


查看答案和解析>>
科目:高中化学 来源:不详 题型:推断题

查看答案和解析>>
科目:高中化学 来源:不详 题型:推断题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
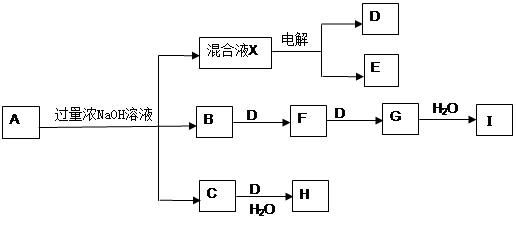
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
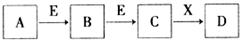
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
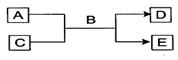
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com