

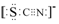 .
.分析 (1)①氯气的发生装置可以依据原料的状态和反应条件选择,一般实验室中利用浓盐酸和二氧化锰加热反应生成;
②欲收集一瓶干燥纯净的氯气,制备出的氯气含氯化氢和水蒸气,通过饱和食盐水除去氯化氢,通过浓硫酸除去水蒸气;
(2)氯气通入氢氧化钠溶液发生反应生成氯化钠、次氯酸钠和水;
(3)①根据SCN-的电子式为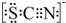 可知,SCN-中碳显+4价,硫显-2价,氮显-3价,碳已经是最高正价了,不能再被氧化了,据此答题;
可知,SCN-中碳显+4价,硫显-2价,氮显-3价,碳已经是最高正价了,不能再被氧化了,据此答题;
②加入用盐酸酸化的BaCl2溶液,产生白色沉淀,说明白色沉淀为硫酸钡,即溶液中有硫酸根离子,其中硫显+6价,而原来SCN-中硫显-2价,所以被氧化的元素为硫元素,据此答题;
③利用硝酸根离子在酸性条件下有强氧化性,遇到铜被还原,生成一氧化氮,在空气中被 氧化成红棕色的二氧化氮气体,可以检验硝酸根离子的存在,据此答题;
④SCN-与Cl2反应生成硫酸根和硝酸根还有二氧化碳,结合电子守恒、原子守恒和电荷守恒写出离子方程式;
解答 解:(1)①实验室中利用浓盐酸和二氧化锰加热反应生成氯气,固体和液体加热制备气体选择装置B,反应的化学方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,
故答案为:B;MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
②利用浓盐酸和二氧化锰制备氯气,欲收集一瓶干燥纯净的氯气,制备出的氯气含氯化氢和水蒸气,通过饱和食盐水除去氯化氢,通过浓硫酸除去水蒸气,选择上图中的装置,其连接顺序为:a i h d e f g j,
故答案为:a i h d e f g j;
(2)氯气通入氢氧化钠溶液发生反应生成氯化钠、次氯酸钠和水,反应的离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
(3)①根据SCN-的电子式为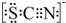 可知,SCN-中碳显+4价,硫显-2价,氮显-3价,碳已经是最高正价了,不能再被氧化了,
可知,SCN-中碳显+4价,硫显-2价,氮显-3价,碳已经是最高正价了,不能再被氧化了,
故答案为:SCN-中的碳元素是最高价态+4价;
②加入用盐酸酸化的BaCl2溶液,产生白色沉淀,说明白色沉淀为硫酸钡,即溶液中有硫酸根离子,其中硫显+6价,而原来SCN-中硫显-2价,所以被氧化的元素为硫元素,故答案为:硫元素;
③利用硝酸根离子在酸性条件下有强氧化性,遇到铜被还原,生成一氧化氮,在空气中被 氧化成红棕色的二氧化氮气体,可以检验硝酸根离子的存在,据此可知实验方案为:取足量铜粉于试管中,加入A中黄色溶液和一定量的稀盐酸,加热,观察到试管上方有红棕色气体生成,证明A中存在,SCN-中氮元素被氧化成,
故答案为:取足量铜粉于试管中,加入A中黄色溶液和一定量的稀盐酸,加热,观察到试管上方有红棕色气体生成,证明A中存在,SCN-中氮元素被氧化成;
④SCN-与Cl2反应生成硫酸根和硝酸根还有二氧化碳,所以它们反应的化学方程式为SCN-+8Cl2+9H2O=NO3-+SO42-+CO2+Cl-+18H+,
故答案为:SCN-+8Cl2+9H2O=NO3-+SO42-+CO2+Cl-+18H+.
点评 本题是实验方案的综合题,综合性较强,其中涉及到了离子的检验、氧化还原的离子方程式的书写、实验步骤的设计、化学计算等知识点,解题的关键是要掌握元素化合物的基础知识及实验基本操作要求.


 全优测试卷系列答案
全优测试卷系列答案 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 氯气可以使湿润的有色布条褪色,是因为氯气具有漂白性 | |
| B. | 分别用盛满HCl气体和盛满NO2气体的烧瓶做喷泉实验,喷泉结束后,所得溶液的物质的量浓度相同 | |
| C. | 向50 mL 18 mol•L-1 的H2SO4溶液中加入足量的铜片加热充分反应后,被还原的H2SO4的物质的量等于0.45 mol | |
| D. | 常温下,浓硝酸可以用铝制容器贮存,说明铝与浓硝酸不反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
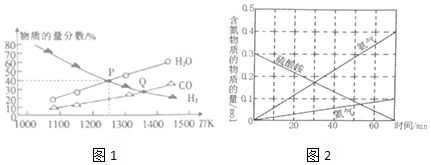
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | 只有⑥ | C. | 只有⑤ | D. | ④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
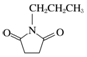 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
的合成路线流程图(无机试剂任选).合成路线流程图示例如下:查看答案和解析>>
科目:高中化学 来源: 题型:推断题
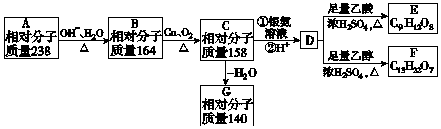
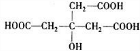 .
.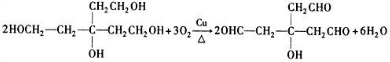 .
.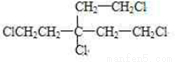 .
.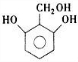 、
、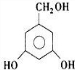 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
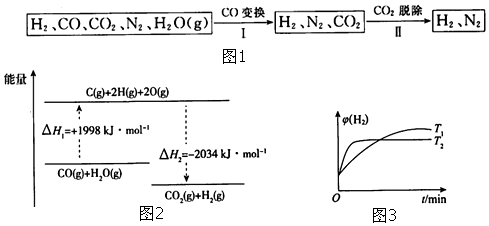
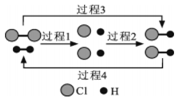 H2 能在Cl2中燃烧生成 HCl,HCl也能在一定条件下分解为H2和Cl2. 图为H2、Cl2和HCl 三者相互转化的微观过程示意图,下列属于吸热过程的是 ( )
H2 能在Cl2中燃烧生成 HCl,HCl也能在一定条件下分解为H2和Cl2. 图为H2、Cl2和HCl 三者相互转化的微观过程示意图,下列属于吸热过程的是 ( )| A. | 过程 1 | B. | 过程 2 | C. | 过程 3 | D. | 过程 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生成 0.1 NA 根共价键 | B. | 消耗反应物总体积 2.24L | ||
| C. | 转移了 2 NA 个电子 | D. | 产物溶于水后,溶液 pH=1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com