
用FeS2纳米材料制成的高容量锂电池,电极分别是二硫化亚铁和金属锂,电解液是含锂盐的有机溶剂。下列说法错误的是
A.金属锂作电池的负极
B.电池正极反应为FeS2+4Li++4e-==Fe+2Li2S
C.放电时,Li+向负极迁移
D.电池总反应为FeS2+4Li ==Fe+2Li2S
 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案科目:高中化学 来源:2017届广东省深圳市三校高三上学期第一次联考化学卷(解析版) 题型:实验题
利用铝灰(主要成分为Al、Al2O3、AlN、FeO等)制备铝鞣剂【主要成分为Al(OH)2Cl】的一种工艺如下:
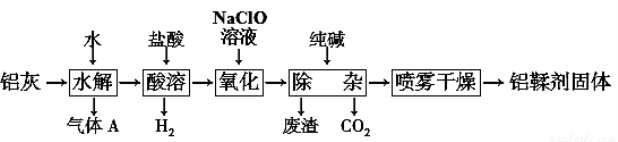
⑴气体A能使湿润的红色石蕊试纸变蓝。铝灰在90 ℃水解生成A的化学方程式为: 。
⑵“酸溶”时,Al2O3发生反应的离子方程式为: 。
⑶“氧化”时,发生反应的离子方程式为: 。
⑷“废渣”成分为________(填化学式)。
⑸采用喷雾干燥而不用蒸发的原因是______________________。
⑹煅烧硫酸铝铵晶体,发生的主要反应为:
4[NH4Al(SO4)2·12H2O]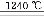 2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O
2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O
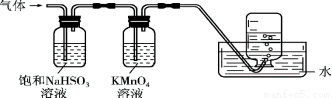
将产生的气体通过如下图所示的装置。则集气瓶中收集到的气体是 (填化学式)。
查看答案和解析>>
科目:高中化学 来源:2017届广东省汕头市高三上学期期末化学试卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数的数值,下列说法正确的是
A.34gH2O2中含有的阴离子数为1NA
B.4.6g乙醇中含有的C-H键的个数为0.6NA
C.标准状况下,VL水含有的氧原子个数约为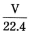
D.1molFe2+与足量的H2O2溶液反应,转移NA个电子
查看答案和解析>>
科目:高中化学 来源:2017届广东省清远市清城区高三上期末B卷化学试卷(解析版) 题型:选择题
在2NO2?N2O4的可逆反应中,下列状态属于平衡状态的是( )
A.υ正=υ逆≠0时的状态 B.NO2全部转变成N2O4的状态
C.c(NO2)=c(N2O4)的状态 D.体系的颜色发生变化的状态
查看答案和解析>>
科目:高中化学 来源:2017届四川省绵阳市高三1月诊断性考试化学试卷(解析版) 题型:实验题
电石广泛用于生产PVC、维尼纶等,电石与水反应所得残渣——电石渣,主要含Ca(OH)2、CaCO3及少量其他杂质。某工业电石渣的几种回收利用流程如下:
几种物质在水中的溶解度曲线如右图。回答下列问题:
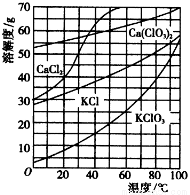
(1)常温氯化
①反应的化学方程式是 。
②提高Cl2转化为Ca(ClO)2的转化率可行的措施有_______(填序号)。
A.加热升高温度 B.适当减缓通入Cl2速率
C.充分搅拌浆料 D.加水使Ca(OH)2完全溶解
③电石渣中的有害杂质CN-与ClO-反应转化为两种无害的气体,每转化1 mol CN-至少需要消耗氧化剂ClO-_______mol。
(2)75 ℃氯化
①生成氯酸钙中氯的化合价为 ,氯化完成后过滤,滤渣的主要成分为______(填化学式)。
②氯酸钙能与KCl反应转化为氯酸钾的原因是 。
(3)有机反应
首先生成氯代乙醇,其结构简式为 ,氯代乙醇再与Ca(OH)2反应生产环氧乙烷。总反应的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源:2017届山东省潍坊市临朐县高三12月阶段测化学试卷(解析版) 题型:实验题
碱式碳酸钴[ Cox(OH)y(CO3)2 ]常用作电子材料,磁性材料的添加剂,受热时可分解生成三种氧化物。为了确定其组成,某化学兴趣小组同学设计了如图所示进行实验。

⑴请完成下列实验步骤:
①称取3.65g样品置于硬质玻璃管内,称量乙、丙装置的质量;
②按如图所示装置组装好仪器,并检验装置气密性;
③加热甲中玻璃管,当乙装置中___________(填实验现象),停止加热;
④打开活塞a,缓缓通入空气数分钟后,称量乙、丙装置的质量;
⑤计算。
⑵步骤④中缓缓通入空气数分钟的目的是_________ _________。
_________。
⑶某同学认为上述实验装置中存在一个明显缺陷,为解决这一问题,可选用下列装置中的_____ _(填字母)连接在_____ ____(填装置连接位置)。
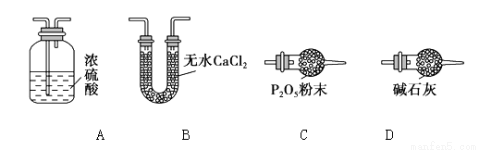
⑷若按正确装置进行实验,测得如下数据:
乙装置的质量/g | 丙装置的质量/g | |
加热前 | 80.00 | 62.00 |
加热后 | 80.36 | 62.88 |
则该碱式碳酸钴的化学式为____________________。
⑸CoCl2·6H2O常用作多彩水泥的添加剂,以含钴废料(含少量Fe、Al等 杂质)制取CoCl2·6H2O的一种工艺如下:
杂质)制取CoCl2·6H2O的一种工艺如下:
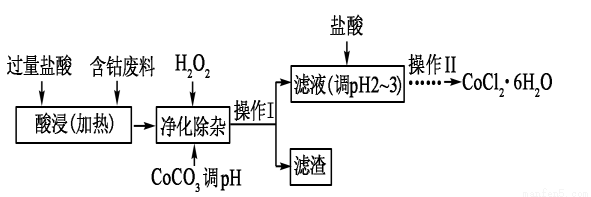
已知:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
开始沉淀(PH) | 2.3 | 7.5 | 7.6 | 3.4 |
完全沉淀(PH) | 4.1 | 9.7 | 9.2 | 5.2 |
①净除杂质时,加入H2O2 发生反应的离子方程式为______________________。
②加入CoCO3调PH为5.2~7.6,则操作Ⅰ获得的滤渣成分为__________________。
③加盐酸调整PH为2~3的目的为____________________________。
查看答案和解析>>
科目:高中化学 来源:2017届山东省潍坊市临朐县高三12月阶段测化学试卷(解析版) 题型:选择题
下列有关说法中正确的是
A. 1 mol/L的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-)
B. 有甲、乙两醋酸溶液,测得甲的pH=a,乙的pH=a+1,若用于中和等物质的量浓度等体积的NaOH溶液,需甲、乙两酸的体积V (乙)>10V(甲)
C. 常温下中和等体积、pH相同的CH3COOH和HCl溶液,消耗NaOH的量相同
D. 将pH=3的醋酸稀释为pH=4的过程中,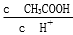 比值不变
比值不变
查看答案和解析>>
科目:高中化学 来源:2017届湖南省株洲市高三上教学质检一化学试卷(解析版) 题型:填空题
如图为KNO3和NaCl的溶解度曲线,请回答下列问题:
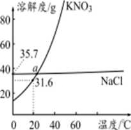
(1)20℃时, KNO3的溶解度为 。
(2)a点处KNO3和NaCl两种溶液中溶质的质量分数 (填“相等”或“不相等”)
(3)若固体KNO3中混有的少量NaCl,可采用 (填“蒸发结晶”或“降温结晶“)的方法提纯。
(4)40℃时,将35.0gNaCl溶于100g水中,降温至0℃时,可析出晶体 g。
查看答案和解析>>
科目:高中化学 来源:2017届湖北省荆门市高三元月调考理综化学试卷(解析版) 题型:推断题
【化学——选修3:物质结构与性质】原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36。已知X的一种1∶2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子的s能级与p能级电子数相等;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,原子中只有一个未成对电子。
(1)Y原子核外共有________种不同运动状态的电子,基态T原子有________种不同能级的电子。
(2)X、Y、Z的第一电离能由小到大的顺序为________(用元素符号表示)。
(3)由X、Y、Z形成的离子ZXY-与XZ2互为等电子体,则ZXY-中X原子的杂化轨道类型为__________________。
(4)Z与R能形成化合物甲,1 mol甲中含________ mol化学键,甲与氢氟酸反应,生成物的分子空间构型分别为_________________________。
(5)G、Q、R氟化物的熔点如下表,造成熔点差异的原因为___________________。
氟化物 | G的氟化物 | Q的氟化物 | R的氟化物 |
熔点/K | 993 | 1 539 | 183 |
(6)向T的硫酸盐溶液中逐滴加入Y的氢化物的水溶液至过量,反应过程中的离子方程式
为________________________;________________________。
(7)X单质的晶胞如图所示,一个X晶胞中有________个X原子;
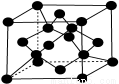
若X晶体的密度为ρ g·cm-3,阿伏加德罗常数的值为NA,则该晶胞的体积为________ cm3 (用代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com