
硫化氢(H2S)的转化是资源利用和环境保护的重要研究课题。
(1)H2S和CO混合加热可制得羰基硫(COS)。羰基硫可作粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。反应方程式为:
CO(g)+H2S(g)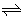 COS(g)+H2(g)
COS(g)+H2(g)
①羰基硫的电子式为_________其含有的共价键类型是________共价键。
②下列能说明碳与硫两元素非金属性相对强弱的是_____________。
a.相同条件下水溶液的pH:Na2CO3 > Na2SO4
b.酸性:H2SO3 > H2CO3
c.S与H2的化合比C与H2的化合更容易
(2)H2S具有还原性,在酸性条件下,能与KMnO4反应生成S、MnSO4、K2SO4和H2O,写出该反应的化学方程式__________________。
(3)H2S气体溶于水形成的氢硫酸是一种二元弱酸,25℃时,在0.10mol·L-1 H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图所示(忽略溶液体积的变化、H2S的挥发)。
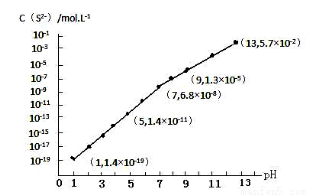
①pH=13时,溶液中的c(H2S)+c(HS-)=____________mol·L-1。
②某溶液含0.020 mol·L-1Mn2+、0.10 mol·L-1H2S,当溶液pH=____________时,Mn2+开始沉淀。[已知:Ksp(MnS)=2.8×10-13]。
(4)H2S的废气可用烧碱溶液吸收,将烧碱吸收H2S后的溶液加入到如图所示的电解池的阳极区进行电解。电解过程中阳极区发生如下反应:
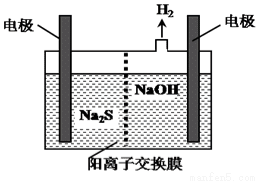
S2--2e-=S↓ (n-1)S+S2- Sn2-
Sn2-
①写出电解时阴极的电极反应式:______________________。
②Na2S溶液中离子浓度由大到小顺序:________________________。
科目:高中化学 来源:2017届湖北省沙市高三上学期第三次考试化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
①0.1 mol·L-1NaAlO2溶液:H+、Na+、Cl-、SO42-
②pH=11的溶液中:CO32-、Na+、AlO2-、NO3-、S2-、SO32-
③水电离的H+浓度为10-12mol·L-1的溶液中:Cl-、CO32-、NO3-、SO32-
④加入Mg能放出H2的溶液中:Mg2+、NH4+、Cl-、K+、SO42-
⑤使甲基橙变黄的溶液中:Fe2+、MnO4-、NO3-、Na+、SO42-
⑥中性溶液中:Fe3+、Al3+、NO3-、Cl-、S2-
A.①③⑤ B.②④ C.②⑤⑥ D.④⑤
查看答案和解析>>
科目:高中化学 来源:2017届广东省高三上学期摸底考试理综化学试卷(解析版) 题型:选择题
化学与社会发展以及人们生活质量的提高有密切关系。下列的叙述不正确的是
A.在1个标准大气压下,水只有在100℃时才能蒸发
B.用13C或14C示踪原子可以进行幽门螺旋杆菌的检测
C.用NaHCO3溶液可以洗去蔬菜、水果等的残留农药
D.使用含钙、镁离子浓度较大的地下水洗衣服,肥皂去污能力会减弱
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上学期开学考试化学试卷(解析版) 题型:选择题
下列有关化学用语正确的是( )
①乙烯的最简式C2H4 ②乙醇的结构简式C2H6O
③四氯化碳的电子式 
 ④乙炔的结构简式CHCH
④乙炔的结构简式CHCH
⑤乙烷的结构式CH3CH3 ⑥乙醛的结构简式CH3COH.
A.③④⑤ B.③④⑥ C.全错 D.全对
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上学期开学考试化学试卷(解析版) 题型:选择题
下列叙述正确的是( )
A.升高温度活化能降低
B.乙醇和汽油都是可再生能源,应大力推广“乙醇汽油”
C.用电解水的方法制取大量氢气可以缓解能源不足的问题
D.推广使用太阳能、风能、海洋能、氢能,有利于缓解温室效应
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上适应性考试(一)理综化学试卷(解析版) 题型:选择题
下列说法错误的是( )
A.等物质的量的NaX和弱酸HX混合后的溶液中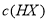 可能大于
可能大于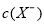
B.在pH=4.5的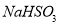 溶液中,
溶液中,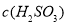 大于
大于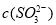
C.向0.1 mol/L醋酸溶液中加入稀释的过程中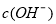 不断增大
不断增大
D.0.1 mol·L—1 某一元酸HA溶液中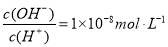 ,则该溶液中由水电离出的
,则该溶液中由水电离出的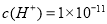
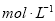
查看答案和解析>>
科目:高中化学 来源:2017届安徽省六安市高三上第一次月考化学试卷(解析版) 题型:推断题
有一瓶澄清溶液,其中可能含有NH4+、K+、Ba2+、Al3+、Fe3+、Mg2+、I-、NO3-、CO32-、SO42-、AlO2-。取该溶液进行以下实验:
①用PH试纸检验,溶液呈强酸性;
②取溶液适量,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色;
③另取溶液适量,逐滴加入NaOH溶液:a.溶液从酸性变为碱性;b.溶液逐渐产生沉淀
c.沉淀完全溶解;d.最后加热溶液,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
其中产生沉淀的物质的量(n)与加入氢氧化钠溶液的体积(V)的关系如下图所示。

④取适量③得到的碱性溶液,加入Na2CO3溶液,有白色沉淀生成。
根据上述实验现象,回答下列问题。
(1)由①可以排除 的存在。
(2)由②可以证明 的存在;同时排除 的存在;
(3)由①③可以推知该溶液中一定含有的阳离子是 ,它们的物质的量浓度比为 。
(4)由④可以证明 的存在,同时排除 的存在。
查看答案和解析>>
科目:高中化学 来源:2017届安徽省淮北市濉溪县高三上学期9月月考化学试卷(解析版) 题型:计算题
实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低,最低可以还原到?3价。某同学取一定量的铁铝合金与一定量很稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4mol·L-1的NaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。试回答下列问题:

⑴ 写出该合金中铁与硝酸反应的离子方程式 ;
⑵ 图中OC段无沉淀生成,此阶段反应的离子方程式为 ;
⑶ DE段发生反应的离子方程式为 ;
⑷ B与A的差值为____________ mol;
⑸ B点对应的沉淀的物质的量为 mol,C点对应的NaOH溶液的体积为_________mL。
查看答案和解析>>
科目:高中化学 来源:2017届河南省灵宝市高三上学期9月月考化学试卷(解析版) 题型:实验题
铝用途广泛,用铝土矿(主要成分为Al2O3·nH2O、少量SiO2和Fe2O3)制取Al有如下途径:
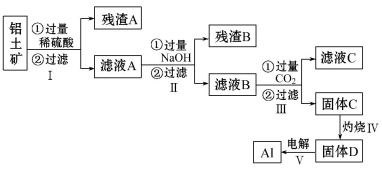
(1)滤液A可用于净水,其净水原理用离子方程式表示为_________________。
(2)灼烧时盛放药品的仪器名称是______________
(3)步骤Ⅴ中发生反应的化学方程式是________________________。
(4)步骤Ⅲ中生成固体C的离子反应方程式为__________________________。
(5)取滤液B 100 mL,加入1 mol/L盐酸200 mL,沉淀量达到最大且质量为11.7 g。则滤液B中c(Al O2-)=_____________。(4分)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com