
【题目】请完成下列问题:
(1)画出氯原子结构示意图;
(2)写出小苏打的化学式;
(3)写出实验室制氯气的离子方程式;
(4)写出红热的木炭与浓硫酸反应的化学方程式 .
【答案】
(1)![]()
(2)NaHCO3
(3)MnO2+2Cl﹣+4H+ ![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
(4)C+2H2SO4(浓) ![]() CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
【解析】解:(1.)氯原子的核内有17个质子,带1 7个正电荷,核外有17个电子,故原子结构示意图为 ![]() ,所以答案是:
,所以答案是: ![]() ;(2.)碳酸氢钠俗称小苏打,化学式为NaHCO3 , 所以答案是:NaHCO3;
;(2.)碳酸氢钠俗称小苏打,化学式为NaHCO3 , 所以答案是:NaHCO3;
(3.)实验室用二氧化锰和浓盐酸加热制取氯气,二氧化锰将浓盐酸氧化为氯气,二氧化锰被还原为氯化锰,同时有水生成,故化学方程式为:MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,离子方程式为MnO2+2Cl﹣+4H+
MnCl2+Cl2↑+2H2O,离子方程式为MnO2+2Cl﹣+4H+ ![]() Mn2++Cl2↑+2H2O,所以答案是:MnO2+2Cl﹣+4H+
Mn2++Cl2↑+2H2O,所以答案是:MnO2+2Cl﹣+4H+ ![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
(4.)木炭在加热条件下被浓硫酸氧化为二氧化碳,浓硫酸被还原为二氧化硫,还有水生成,故化学方程式为C+2H2SO4(浓) ![]() CO2↑+2SO2↑+2H2O,所以答案是:C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O,所以答案是:C+2H2SO4(浓) ![]() CO2↑+2SO2↑+2H2O.
CO2↑+2SO2↑+2H2O.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】硫酸工业在国民经济中占有极其重要的地位。
(1)硫酸的最大消费渠道是化肥工业,用硫酸制造的常见化肥有(任写一种)。
(2)硫酸生产中,根据化学平衡原理来确定的条件或措施有________(填写序号)。
A.矿石加入沸腾炉之前先粉碎
B.使用V2O5作催化剂
C.转化器中使用适宜的温度
D.净化后的炉气中要有过量的空气
E.催化氧化在常压下进行
F.吸收塔中用98.3%的浓硫酸吸收SO3
(3)在硫酸工业中,通过下列反应使二氧化硫转化为三氧化硫:2SO2(g)+ ![]() O2(g)
O2(g) ![]() 2SO3(g) ΔH=-98.3 kJ·mol-1。在实际工业生产中,常采用“二转二吸法”,即将第一次转化生成的SO3分离后,将未转化的SO2进行二次转化,假若两次SO2的转化率均为95%,则最终SO2的转化率为。
2SO3(g) ΔH=-98.3 kJ·mol-1。在实际工业生产中,常采用“二转二吸法”,即将第一次转化生成的SO3分离后,将未转化的SO2进行二次转化,假若两次SO2的转化率均为95%,则最终SO2的转化率为。
(4)硫酸的工业制法过程涉及三个主要的化学反应及相应的设备(沸腾炉、转化器、吸收塔)。
①三个设备分别使反应物之间或冷热气体之间进行“对流”。请简单描述吸收塔中反应物之间是怎样对流的。。
②工业生产中常用氨-酸法进行尾气脱硫,以达到消除污染、废物利用的目的。用化学方程式表示其反应原理。(只写出2个方程式即可).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加成反应是有机化学中的一类重要的反应,下列过程中发生加成反应的是( )
A. 甲烷与氯气混合后光照条件下发生反应
B. 乙烯通入溴的四氯化碳溶液发生反应
C. 乙烯通入酸性高锰酸钾溶液后溶液褪色
D. 在苯中滴入溴水,振荡后溴水层颜色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如下图所示。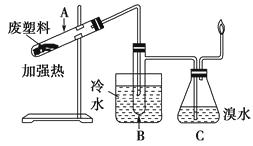
加热聚丙烯废塑料得到的产物如下表:
产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
质量分数/% | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
(1)试管A中残余物有多种用途,如下列转化就可制取高聚物聚乙炔。
A中残留物→聚乙炔
写出反应②③的化学方程式?
(2)B中收集得到的物质中能使酸性KMnO4溶液褪色的物质的一氯代物有种。
(3)锥形瓶C中观察到的现象是。经溴水充分吸收,剩余气体经干燥后平均相对分子质量为。
(4)写出C中逸出的气体在工业上的两种用途、。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢铁工业对促进经济和社会发展起了重要作用。
(1)炼铁高炉分为五部分,铁矿石与高温煤气主要在部分发生反应,在部分开始生成生铁和炉渣。
(2)炼钢时,除磷的化学方程式为;加入硅、锰和铝的目的是。
(3)不锈钢含有的Cr元素是在炼钢过程的氧吹(填“前”或“后”)加入,原因是。
(4)炼铁和炼钢生产中,尾气中均含有的主要污染物是。从环保和经济角度考虑,上述尾气经处理可用作。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组同学对由NaHCO3和KHCO3组成的某均匀混合物进行实验,测得如下数据(盐酸的物质的量浓度相等)
50mL盐酸 | 50mL盐酸 | 50mL盐酸 | |
m(混合物) | 9.2g | 15.7g | 27.6g |
V(CO2)(标况) | 2.24L | 3.36L | 3.36L |
试计算:
(1)混合物与盐酸反应的离子方程式
(2)盐酸的物质的量浓度;
(3)混合物中两物质的物质的量之比.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是人类未来最理想的燃料,以水为原料大量制取氢气的最理想的途径是( )
A. 利用太阳能直接使水分解产生氢气
B. 以焦炭和水制取水煤气(含CO和H2)后分离出氢气
C. 用铁和盐酸反应放出氢气
D. 由热电站提供电力电解水产生氢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2与Cl2的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛.某兴趣小组通过题图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究.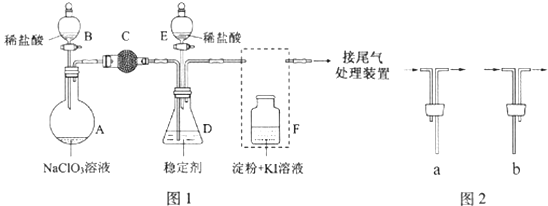
(1)仪器D的名称是 . 安装F中导管时,应选用图2中的 .
(2)打开B的活塞,A中发生反应:2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O.
为使ClO2在D中被稳定剂充分吸收,滴加稀盐酸的速度宜(填“快”或“慢”).
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2 , 此时F中溶液的颜色不变,则装置C的作用是 .
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2 , 该反应的离子方程式为 , 在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com