
��8�֣���1.66 g̼���ƺ��������ƵĹ���������ȫ����ˮ�����ϡ��Һ��Ȼ�������Һ����μ���1 mo1��L-1�����ᣬ�������������������CO2���������״������ϵ��ͼ��ʾ��

��ش��������⣺
��1��OA����������Na2CO3��NaOH�����ķ�Ӧ����Ӧ����Һ�е������� ���ѧʽ����
��2��������B��ʱ������CO2�����Ϊ mL����״������
��3������ԭ�������Na2CO3��������������д����Ҫ������̣��������3λ��Ч���֣�
��8�֣�
��1��NaCl��NaHCO3 ����2�֣����1����1�֣����һ�������֣�
��2��224 ��2�֣�
��3��63.9�G��4�֡����Na2CO3������Ϊ1.06g��2�֣������ȷ�ٸ�2�֡�ֻ�н�����̲��÷֡����㷽����������������֡���
��������
�����������1��̼�������������ƵĻ����Һ�м���ϡ���ᣬ�����������������Ʒ�Ӧ�����Ȼ��ƺ�ˮ������̼���Ʒ�Ӧ����̼�����ƣ����̼�����������ᷴӦ����������̼���壬����OA����Һ�е�����ΪNaCl��NaHCO3 ��
��2����ͼ��֪���ɶ�����̼������������Ϊ35-25=10mL������NaHCO3��HCl��CO2�������������̼�����ʵ�����0.01L��1mol/L=0.01mol����״���µ������0.01mol��22.4L/mol=224mL��
��3������CԪ���غ㣬�������̼���Ƶ����ʵ���Ϊ0.01mol��������0.01mol��106g/mol=1.06g����ԭ�������Na2CO3����������Ϊ1.06g/1.66g��100%=63.9%��
���㣺�����̼���⡢��������������ķ�Ӧ�ļ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�����и�����ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
�����������ڵ���ʵ���
A��ͭ B������ C���������� D������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�����и߶���ѧ����ĩ���Ի�ѧ��B���Ծ��������棩 ���ͣ�ѡ����
ˮ��Һ���ܴ��������һ��������
A��Na����Ca2����Cl����SO42�� B��Mg2����NH��Cl����SO42��
C��K����Fe3����NO3����SCN�� D��Fe2����H����SO32����ClO��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�����и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ܴﵽʵ��Ŀ�ĵ���
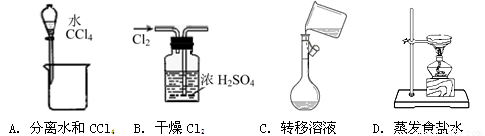
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�����и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���л�ѧ����ʽ�У����������ӷ���ʽH++OH-��H2O��ʾ����
A��2NaOH + H2SO4 = Na2SO4+2H2O
B��Ba��OH��2 +2HCl = BaCl2+2H2O
C��Cu��OH��2 + 2HNO3 =Cu��NO3��2 +2H2O
D��KOH+ HCl = KCl+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�ӱ�ʡ�����и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ������
��10�֣�Χ�������������ʣ���������A12O3����ϡ���ᡢ��H2SO4����Ba(OH)2���塢��ϡ��ˮ����A12(SO4)3������Ҫ��ش��������⡣
��1��������ǿ�ᷴӦ��������ǿ�Ӧ���� ������ţ���
��2�����ڵ���ʵ��� ������ţ���
��3��д����������ȡAl(OH)3�����ӷ���ʽ�� ��
��4�������ʼ䷢����Ӧ�����ӷ���ʽΪH++OH- �� H2O����д���÷�Ӧ�Ļ�ѧ����ʽ�� ��
��5��34.2g������ˮ���500mL��Һ������Һ��SO42-�����ʵ���Ũ��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�ӱ�ʡ�����и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�˶�����ʹ�õķ���ǹ���õġ���ҩ���ɷ�������غͺ��ף���ײ������������ͬʱ�������̡�ײ��ʱ������Ӧ�Ļ�ѧ����ʽΪ��5KClO3��6P��3P2O5��5KCl���������й������������
A��������Ӧ��Cl�Ļ��ϼ��ɣ�5�۱�Ϊ��1��
B��P2O5��P����ԭ�����õIJ���
C���÷�Ӧ�б���ԭ�뱻�������ʵ����ʵ���֮��Ϊ5��6
D��������Ӧ������3mol Pʱ��ת�Ƶ��ӵ����ʵ���Ϊ15mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�ӱ�ʡ�����и߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ������
��8�֣������������ܱ������ͨ��x mol H2(��)��y mol I2(��)��������Ӧ��
H2(g)+I2(g) 2HI(g) ��H<0
2HI(g) ��H<0
�ı�����������Ӧ���ʽ���θı�?���������С�����䡱��
��1�������¶� �� ��2��������� ��
��3����������H2 �� ��4�������ݻ����䣬ͨ������ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㶫ʡտ���и߶���һѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�������
��һ���¶��£���10 L�ܱ������г���5.2 mol NO2���ﵽƽ��ʱ�� c��N2O4��=0.16 mol��L-1��
�������¶��´˷�Ӧ��ƽ�ⳣ��K����������ʽ�ķ���д��������̣���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com