
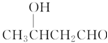
| A. | ①③④ | B. | ②④⑤ | C. | ①③⑤ | D. | ①②⑤ |
分析 含有羧基或羟基的有机物能发生酯化反应,含有碳碳不饱和键、苯环、醛基、羰基的有机物能发生加成反应,烃、醇、醛、羧酸等有机物都能发生氧化反应,据此分析解答.
解答 解:①CH2=CHCOOH中含有碳碳双键和羧基,所以能发生加成反应、酯化反应和氧化反应,故正确;
②CH2=CHCOOCH3中不含羧基和羟基,则不能发生酯化反应,故错误;
③CH2=CHCH2OH中含有碳碳双键和醇羟基,所以能发生加成反应、酯化反应和氧化反应,故正确;
④CH3CH2CH2OH中不含碳碳不饱和键或醛基、苯环及羰基,所以不能发生加成反应,故错误;
⑤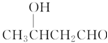 中醇羟基和醛基能发生氧化反应,醇羟基能发生酯化反应,醛基能发生加成反应,故正确;
中醇羟基和醛基能发生氧化反应,醇羟基能发生酯化反应,醛基能发生加成反应,故正确;
故选C.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,侧重考查醇、醛、羧酸等有机物的性质,知道常见官能团及其反应类型关系,题目难度不大.


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:多选题
| A. | 向CuSO4溶液中加入Na2O2:2Na2O2+Cu2++H2O═4 Na++Cu(OH)2↓+O2↑ | |
| B. | 工业上用石灰乳制备漂白粉:Ca+2OH-+Cl2=Ca2++ClO-+Cl-+H2O | |
| C. | 向Na2SiO3溶液中通入过量SO2:SiO32-+2SO2+2H2O═H2SiO3↓+2HSO3- | |
| D. | 制备Fe(OH)3胶体:Fe3++3H2O═Fe(OH)3(胶体)+3H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
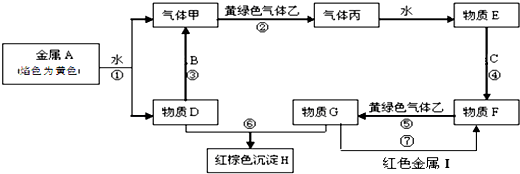
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯使酸性高锰酸钾褪色的原理和使溴水褪色的原理相同 | |
| B. | 乙烯不能合成高分子化合物 | |
| C. | 工业制备乙烯通常通过石油的裂解 | |
| D. | 聚乙烯能使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CS2与NO2 | B. | SO2与N2O | C. | SO2与O3 | D. | PCl3与BF3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 花生油 | 亚麻仁油 | 牛油 | 黄油 | 硬化大豆油 | 大豆油 | |
| 皂化值 | 190 | 180 | 195 | 226 | 193 | 193 |
| 碘值 | 90 | 182 | 38 | 38 | 5 | 126 |
 的酯,若皂化值为430,求n为4.
的酯,若皂化值为430,求n为4.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com