
 计算水的物质的量,根据方程式计算生成的气体,再根据N=nNA计算分子数目.
计算水的物质的量,根据方程式计算生成的气体,再根据N=nNA计算分子数目. 计算32gO-2离子的物质的量,每个O-2离子含有17个电子,根据N=nNA计算电子数目.
计算32gO-2离子的物质的量,每个O-2离子含有17个电子,根据N=nNA计算电子数目. ,起还原剂作用的H2O2中氧元素化合价由-1价升高为0价,据此计算.
,起还原剂作用的H2O2中氧元素化合价由-1价升高为0价,据此计算. 计算碳酸钠的物质的量,每摩尔碳酸钠含有3mol离子,根据N=nNA计算离子数目.
计算碳酸钠的物质的量,每摩尔碳酸钠含有3mol离子,根据N=nNA计算离子数目. 2H2O+O2↑,H2O2起还原剂与氧化剂作用,各占
2H2O+O2↑,H2O2起还原剂与氧化剂作用,各占 ,起还原剂作用的H2O2中氧元素化合价由-1价升高为0价,0.01mol×
,起还原剂作用的H2O2中氧元素化合价由-1价升高为0价,0.01mol× ×2×NAmol-1=0.01NA,故C错误;
×2×NAmol-1=0.01NA,故C错误;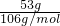 =0.5mol,每摩尔碳酸钠含有3mol离子,所以含有离子数为0.5mol×3×NAmol-1=1.5NA,故D正确.
=0.5mol,每摩尔碳酸钠含有3mol离子,所以含有离子数为0.5mol×3×NAmol-1=1.5NA,故D正确.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
A.1 L 1 mol·L-1 CH3COONa溶液中存在NA个CH3COO-离子
B.1 mol CnH2n+2含有(3n+1)NA个共价键
C.1 mol Cl2参加化学反应获得的电子数都是2NA
D.1 mol NO2气体降温后颜色变浅,其所含的分子数仍为NA
查看答案和解析>>
科目:高中化学 来源:2014届山东省高一上学期期末考前考试化学试卷 题型:选择题
设NA表示阿伏加德罗常数值,下列叙述正确的是
A.NA个氧气分子和NA个氢气分子的质量比为16∶1
B.标准状况下,22.4LH2O含有的分子数为NA
C.11.2L 氯气中含有的原子数为NA个
D.2L 1mol/L Na2SO4溶液中Na+离子数为2NA个
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com