
【题目】实验室里需要纯净的NaCl溶液,但手边只有混有Na2SO4、NaHCO3的NaCl。某学生设计了如图所示方案提取纯净的NaCl溶液。
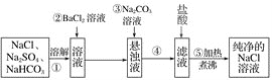
如果此方案正确,那么:
(1)操作④为________,操作①、④、⑤都用到的玻璃仪器有____________。
(2)操作②为什么不用硝酸钡溶液,其理由是___________________________________。
(3)进行操作②后,如何判断SO42-已除尽,方法是_______________________________。
(4)操作③的目的是____________,为什么不先过滤后加碳酸钠溶液?理由是____________。
(5)操作⑤的目的是____________。
【答案】过滤 烧杯、玻璃棒 溶液中引入新的杂质离子NO3— 取少量上层清液加入BaCl2溶液,若无白色沉淀说明SO42—已除尽 除去过量的Ba2+ 先加Na2CO3然后过滤,可以减少一次过滤操作 除去溶解在溶液中的HCl
【解析】
混合物溶解后加入氯化钡可生成硫酸钡沉淀,过滤后得到滤液含有氯化钠、氯化钡、碳酸氢钠,加入碳酸钠溶液生成碳酸钡沉淀,过滤,滤液中含有碳酸钠、碳酸氢钠和氯化钠,加入盐酸,盐酸和碳酸钠、碳酸氢钠均反应生成氯化钠、水和二氧化碳,加热煮沸,可得到纯净的氯化钠溶液,以此解答该题。
(1)加入碳酸钠后有碳酸钡沉淀产生,除去碳酸钡的方法是过滤,则操作④为过滤;操作①、④、⑤分别是溶解、过滤、蒸发,因此都用到的玻璃仪器有烧杯、玻璃棒。
(2)加入硝酸钡溶液,硝酸钡和硫酸钠反应生成硫酸钡和硝酸钠,除去了硫酸钠,但引入了硝酸钠等新的杂质,因此操作②不用硝酸钡溶液。
(3)加入过量氯化钡溶液除去硫酸根离子,检验硫酸根离子已全部沉淀的判断方法为取少量上层清液加入BaCl2溶液,若无白色沉淀说明SO42—已除尽。
(4)操作③加入碳酸钠溶液,碳酸钠与过量的氯化钡反应生成碳酸钡和氯化钠,目的是除去溶液中过量的Ba2+,先加Na2CO3然后过滤,可以减少一次过滤操作,所以不先过滤后加碳酸钠溶液。
(5)由于盐酸过量,则操作⑤的目的是除去溶解在溶液中的HCl。


科目:高中化学 来源: 题型:
【题目】A、B、C、D 均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如下图所示(反应条件及其他物质已经略去):
![]()
(1)若 A 是一种金属,C 是淡黄色固体,C 的阴阳离子个数比为_______;
(2)若 A 为淡黄色固体单质,写出 D 的浓溶液与铜反应的化学方程式_______;
(3)若 A 是化合物,C 是红棕色气体,则 A 的化学式为_____;C 转化为 D 的过程中,氧化剂与还原剂的质量比为_____。
(4)若 A 为黑色固体单质,C 是空气中的主要温室气体。C 还可以转化为 A,写出该反应的化学方程 式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制一定物质的量浓度的KOH溶液时,导致浓度偏低的原因可能是( )
A.容量瓶中原有少量的蒸馏水B.移液时,不慎将液体流到瓶外
C.溶解后没有冷却就转移到容量瓶中D.定容时仰视观察刻度线和液面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeSO4受热分解的化学方程式为2FeSO4![]() Fe2O3+SO2↑+SO3↑
Fe2O3+SO2↑+SO3↑
请回答:
(1)将FeSO4受热产生的气体按图示装置进行实验,证实含有SO3和SO2。能说明SO2存在的实验现象是______________________;为测定BaSO4沉淀的质量,后续的操作步骤依次为________、洗涤、干燥、称量。

(2)设计一个实验方案,用化学方法验证FeSO4受热后固体的成分(不考虑其他反应)
________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别称取2.39g(NH4)2SO4和NH4Cl固体混合物两份。
(1)将其中一份配成溶液,逐滴加入一定浓度的Ba(OH)2溶液,产生的沉淀质量与加入Ba(OH)2溶液体积的关系如图。混合物中n[(NH4)2SO4]∶n(NH4Cl)为________。
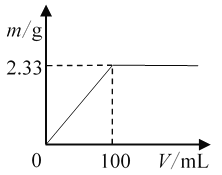
(2)另一份固体混合物中NH与Ba(OH)2溶液(浓度同上)恰好完全反应时,溶液中c(Cl-)=________(溶液体积变化忽略不计)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图装置也可用于检验溴乙烷与氢氧化钠的醇溶液反应生成物乙烯的检验,下列说法不正确的是
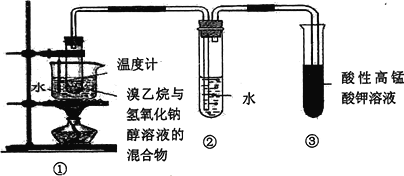
A. 该反应为消去反应 B. 反应实验过程中可观察到酸性KMnO4溶液褪色
C. 可用溴水溶液代替酸性KMnO4溶液 D. 乙烯难溶于水,故此装置②可以省去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下用0.1000mol/L的盐酸分别逐滴加入到20.00mL0.1000mol/L的三种一元碱XOH、MOH、YOH溶液中,溶液的pH随加入盐酸体积的变化如图所示。下列叙述错误的是
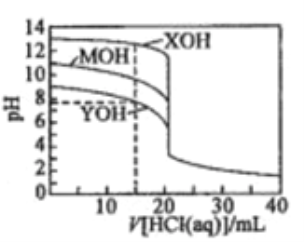
A. XOH为强碱,MOH、YOH均为弱碱
B. V[HCl(aq)]=15.00mL时,三种溶液中离子总浓度大小顺序:XOH>MOH>YOH
C. V[HCl(aq)]=20.00mL时,三种溶液中水的电离程度:XOH>MOH>YOH
D. V[HCl(aq)]=40.00ml.时,YOH溶液中:c(H+)=c(Y+)+c(OH-)+2c(YOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G是制备治疗高血压药物纳多洛尔的中间体,实验室由A制备G的一种路线如下:
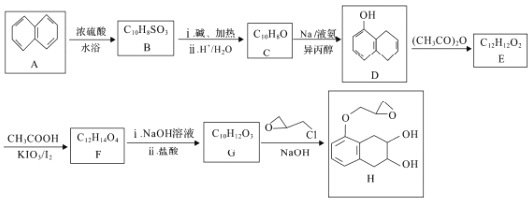
已知:![]()
(1)A的化学名称是________________。
(2)H中所含官能团的名称是____________;有G生成H的反应类型是__________。
(3)C的结构简式为__________,F的结构简式为______________。
(4)由D生成E的化学方程式为___________________________。
(5)芳香族化合物X是F的同分异构体,1molX最多可与4molNaOH反应,其核磁共振氢谱显示分子中有3种不同化学环境的氢,且峰面积比为3:3:1,写出两种符合要求的X的结构简式:___________________________。
(6)写出以甲苯和(CH3CO)2O为原料(其他无机试剂任选)制备化合物![]() 的合成路线:_____________________________________________。
的合成路线:_____________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com