
(1)Na2SO4 (2)Na2SO4和Na2SO3 (3)Na2SO4和NaHSO3
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案科目:高中化学 来源: 题型:

| 温度(K) | 273 | 308 | 373 |
| K(mol?L-1)-1 | 6.78 | 3.13 | 2.78 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A-B | A=B | A≡B | ||
| CO | 键能(kJ/mol) | 357.7 | 798.9 | 1071.9 |
| 键能差值(kJ/mol) | 441.2 273 | |||
| N2 | 键能(kJ/mol) | 154.8 | 418.4 | 941.7 |
| 键能差值(kJ/mol) | 263.6 523.3 | |||
查看答案和解析>>
科目:高中化学 来源:走向清华北大同步导读·高一化学 题型:038
已知273℃、1.01×105Pa时,1mol气体所占的体积为44.8L,现将此条件下的V1 L SO2和O2混合气体通过装有催化剂的反应器,假设反应完全后,气体的体积为V2 L,所得的气体用含a mol NaOH的溶液吸收,恰好完全反应,当产物分别为下列3种情况时,计算并推导a的表达式.(用V1、V2表示)(1)Na2SO4;(2)Na2SO4和Na2SO3;(3)Na2SO4和NaHSO3。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年北京市海淀区高三第二学期适应性练习理综化学试卷(解析版) 题型:填空题
氯气常用于自来水厂杀菌消毒。
(1)工业上用铁电极和石墨做为电极电解饱和食盐水生产氯气,铁电极作 极,石墨电极上的电极反应式为 。
(2)氯氧化法是在碱性条件下,用Cl2将废水中的CN-氧化成无毒的N2和CO2。该反应的离子方程式为 。
(3)氯胺(NH2Cl)消毒法是在用液氯处理自来水的同时通入少量氨气,发生反应:Cl2 + NH3 = NH2Cl + HCl,生成的NH2Cl比HClO稳定,且能部分水解重新生成HClO,起到消毒杀菌的作用。
①氯胺能消毒杀菌的原因是 (用化学用语表示)。
②氯胺消毒法处理后的水中,氮元素多以NH4+的形式存在。
已知:NH4+(aq) + 1.5O2(g)= NO2-(aq) + 2H+(aq) + H2O (l) ΔH=-273 kJ·mol-1
NH4+(aq) + 2O2(g)= NO3-(aq) + 2H+(aq) + H2O (l) ΔH =-346 kJ·mol-1
NO2-(aq)被O2氧化成NO3-(aq)的热化学方程式为 。
(4)在水产养殖中,可以用Na2S2O3将水中残余的微量Cl2除去,某实验小组利用下图所示装置和药品制备Na2S2O3。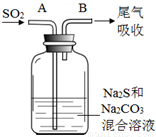
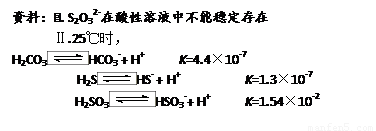
结合上述资料回答:
开始通SO2时,在B口检测到有新的气体生成,判断从B口排出的气体中是否含有H2S,并写出判断依据 。
为获得较多的Na2S2O3,当溶液的pH接近7时,应立即停止通入SO2,其原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com