


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
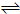 xC(g)达到平衡时,C的体积分数为W%,生成C为amol.当再投1mol A和1mol B重新达平衡.请用大于、小于、等于或不能确定填写在下列条件下从新达到平衡的结果.
xC(g)达到平衡时,C的体积分数为W%,生成C为amol.当再投1mol A和1mol B重新达平衡.请用大于、小于、等于或不能确定填写在下列条件下从新达到平衡的结果.查看答案和解析>>
科目:高中化学 来源:2011-2012学年甘肃省高三上学期第一次检测化学试卷 题型:填空题
(10分)Ⅰ、恒温、恒压下,在一个可变容积的容器中发生如下反应: N2(g)+3H2(g) 2NH3(g); △H<0
2NH3(g); △H<0
(1)工业生产中,该反应通常在高压下进行反应,做出此选择的理由是:
① ;
② 。
(2)开始时放入1mol N2和3mol H2,到达平衡后,生成amol NH3,若开始时放入χmol N2 、3mol H2和y mol NH3,到达平衡后,NH3的物质的量为 3amol,则x= mol,y= mol。
Ⅱ、若该容器恒压、绝热(与外界不发生热交换),在一个与(2)反应前起始条件完全相同的容器中发生上述反应
(3)若开始时放入1mol N2和3mol H2,到达平衡后,生成b mol NH3,将b与(2)小题中的a进行比较 (选填一个编号)
(甲)a<b (乙)a>b (丙)a=b (丁)不能比较a和b的大小
作出此判断的理由是 。
Ⅲ、某研究性学习小组为探究利用电化学原理合成氨,设计如图所示的装置,

(4)电极B为 极
(5)电极A发生的电极反应式为
(6)该电池工作一段时间后,电解质溶液pH
(填增大、减小或不变)
查看答案和解析>>
科目:高中化学 来源:2010-2011学年甘肃省高三第二次联合考试(理综)化学部分 题型:填空题
Ⅰ、恒温、恒压下,在一个可变容积的容器中发生如下反应: N2(g)+3H2(g) 2NH3(g);△H<0
2NH3(g);△H<0
(1)工业生产中,该反应通常在高压下进行反应,做出此选择的理由是:
① ;
② 。
(2)开始时放入1mol N2和3mol H2,到达平衡后,生成amol NH3,若开始时放入χmol N2 、3mol H2和y mol NH3,到达平衡后,NH3的物质的量为 3amol,则x= mol,y= mol。
Ⅱ、若该容器恒压、绝热(与外界不发生热交换),在一个与(2)反应前起始条件完全相同的容器中发生上述反应
(3)若开始时放入1mol N2和3mol H2,到达平衡后,生成b mol NH3,将b与(2)小题中的a进行比较 (选填一个编号)
(甲)a<b (乙)a>b (丙)a=b (丁)不能比较a和b的大小
作出此判断的理由是 。
Ⅲ、某研究性学习小组为探究利用电化学原理合成氨,设计如图所示的装置,

(4)电极B为 极
(5)电极A发生的电极反应式为
(6)该电池工作一段时间后,电解质溶液pH (填增大、减小或不变)
查看答案和解析>>
科目:高中化学 来源:专项题 题型:单选题
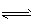 2C(g),一段时间后达到平衡,生成nmol C。则下列说法中正确的是
2C(g),一段时间后达到平衡,生成nmol C。则下列说法中正确的是 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com