
| A. | 用电子式表示氢溴酸的形成过程为: | |
| B. | 乙烯的结构简式:C2H4 | |
| C. | 四氯化碳的电子式为: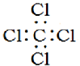 | |
| D. | 质子数为27、中子数为33的Co原子:${\;}_{27}^{60}$Co |
分析 A.HBr为共价化合物;
B.结构简式中碳碳双键不能省略;
C.漏写Cl周围的电子;
D.质子数为27、中子数为33,则质量数为60.
解答 解:A.HBr为共价化合物,则用电子式表示氢溴酸的形成过程为 ,故A错误;
,故A错误;
B.结构简式中碳碳双键不能省略,则乙烯的结构简式为CH2=CH2,故B错误;
C.漏写Cl周围的电子,四氯化碳的电子式为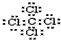 ,故C错误;
,故C错误;
D.质子数为27、中子数为33,则质量数为60,则Co原子为${\;}_{27}^{60}$Co,故D正确;
故选D.
点评 本题考查化学用语,为高频考点,把握电子式、结构简式、原子表示方法、化合物形成过程为解答的关键,侧重分析与应用能力的考查,注意化学用语的区别及规范应用,题目难度不大.


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ | |
| B. | NH4Cl $\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+HCl↑ | |
| C. | 2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3 | |
| D. | Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同一主族元素原子序数越大的单质的熔点、沸点也越高 | |
| B. | 除H外,周期表中主族族序数等于周期数的元素全为金属元素 | |
| C. | 同主族的非金属的简单氢化物中最稳定的其熔、沸点也最高 | |
| D. | 同周期的主族元素形成的简单离子的半径从左到右依次减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ||||||||
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 1:2 | C. | 1:3 | D. | 3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
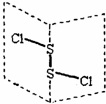 二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2遇水易与水发生反应,并产生能使品红褪色的气体,下列说法中错误的是( )
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2遇水易与水发生反应,并产生能使品红褪色的气体,下列说法中错误的是( )| A. | S2Cl2的结构式为 Cl-S-S-Cl | |
| B. | S2Cl2与水反应时只有S-Cl断裂 | |
| C. | S2Br2含有极性键和非极性键 | |
| D. | S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数:b>a>c>d | B. | 原子半径:C>D>A>B | ||
| C. | 离子半径:Cn->D(n+1)->An+>B(n+1)+ | D. | 单质还原性:A>B>C>D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
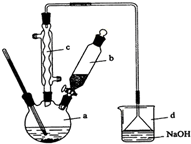 溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如表:
溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如表:| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com