
下列叙述正确的是()
A. 工业上电解熔融的Al2O3冶炼铝用铁做阳极
B. 用惰性电极电解Na2SO4溶液,阴、阳两极产物的物质的量之比为1:2
C. 用惰性电极电解饱和NaCl溶液,若有1mol电子转移,则生成1mol NaOH
D. 用惰性电极电解浓CuSO4溶液一小段时间后,加入Cu2O固体可以使CuSO4溶液恢复原来浓度
考点: 电解原理.
专题: 电化学专题.
分析: A、依据电解原理,铁做阳极,铁失电子生成亚铁离子,使阳极损耗;
B、电解硫酸钠溶液实质电解水,反应中阳极生成氧气,阴极生成氢气;
C、用惰性电极电解饱和NaCl溶液,生成氢氧化钠和氢气、氯气,2mol电子转移反应生成2mol氢氧化钠;
D、电解硫酸铜溶液生成氧气、硫酸和铜,加入CuO恢复溶液浓度,加入Cu2O固体发生氧化还原反应.
解答: 解:A、依据电解原理,铁做阳极,铁失电子生成亚铁离子,使阳极损耗,工业上是利用石墨做电解电解熔融的Al2O3冶炼铝,故A错误;
B、电解硫酸钠溶液实质电解水,反应中阳极生成氧气,阴极生成氢气,阴、阳两极产物的物质的量之比为2:1,故B错误;
C、用惰性电极电解饱和NaCl溶液,生成氢氧化钠和氢气、氯气,2mol电子转移反应生成2mol氢氧化钠,若有1mol电子转移,则生成1mol NaOH,故C正确;
D、电解硫酸铜溶液生成氧气、硫酸和铜,加入CuO恢复溶液浓度,加入Cu2O固体发生氧化还原反应不能恢复溶液浓度,故D错误;
故选C.
点评: 本题考查了电解原理的分析应用,主要是电解过程中产物的分析,氧化还原反应电子转移的计算应用,注意溶液浓度恢复的实质是出什么加什么,题目难度中等.


科目:高中化学 来源: 题型:
(1)实验操作中,不慎将手指划破,这时可从急救箱中取FeCl3溶液止血,其原理是 .
(2)今有两瓶标签模糊不清,只知道分别盛有淀粉溶液和氯化钠溶液,试用2种方法对其鉴别.
① ;② .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有机物分子中,可形成顺反异构的是()
A. CH2=CHCH3 B. CH2=CHCH2CH3 C. CH3CH=C(CH3)2 D. CH3CH=CHCl
查看答案和解析>>
科目:高中化学 来源: 题型:
氢氧化锂(LiAlH4)既是金属储氢材料又是有机合成中常用的试剂,溶于适量的水可得到无色溶液:LiAlH4+2H2O═LiAlO2+4H2↑,在125℃分解为LiH、H2和Al.下列说法不正确的是()
A. LiAlH4中H元素的化合价为﹣1
B. LiAlH4L、iAlO2、LiH均是离子化合物
C. 1mol LiAlH4在125℃完全分解,转移4mol电子
D. 0.5 mol LiAlH4与水充分反应后产生44.8L H2
查看答案和解析>>
科目:高中化学 来源: 题型:
C、O、Si、Cl、Na、Fe是中学化学中常见的六种元素.
(1)Si位于元素周期表第三周期第ⅣA族,Fe2+的离子结构示意图 ,Cl的基态原子外围电子层排布式为 ;
(2)用“>”或“<”填空:
第一电离能 键能 沸点
O Na H﹣Cl H﹣Si CO2 H2O
(3)氯的一种常见含氧酸有漂白性,它与H2CO3酸性强弱不同,写出可以证明此结论一个化学方程式 ;
(4)黄绿色气体二氧化氯(ClO2)是一种高效、广谱、安全的杀菌、消毒剂.工业上常利用氯酸钠和浓盐酸来制备ClO2,同时还得到一种黄绿色的气体单质、一种无色液体和一种常见离子化合物.写出该反应的化学方程式,并标出电子转移的方向和数目: ;
(5)Ti倍称为继铁铝之后“21世纪”金属,应用前景很广.钛铁矿(FeTiO3)可被一氯化碳还原为铁和TiO2固体.在25℃、101KPa下,已知煤消耗7克CO,吸收aKJ热量,该反应的热化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
家用炒菜锅用水清洗后,出现红棕色的锈斑.在此变化过程中不发生的化学反应是()
A. 4Fe(OH)2+2H2O+O2═4Fe(OH)3
B. 2Fe+2H2O+O2═2Fe(OH)2
C. 正极反应:2H2O+O2+4 e﹣→4OH﹣
D. 负极反应:Fe→Fe3++3 e﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,在容积为2L的密闭容器中,将2mol 气体M和3mol N气体混合,发生如下反应:2M(g)+3N(g)⇌x Q(g)+3R(g),该反应达平衡时,生成2.4mol R,并测得Q的浓度为0.4mol/L,下列有关叙述正确的是()
A. x值为2 B. 混合气体的密度增大
C. 平衡时N的浓度为0.3 mol/L D. N的转化率为20%
查看答案和解析>>
科目:高中化学 来源: 题型:
美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电源.氢氧燃料电池的突出优点是把化学能直接转化为电能,而不经过热能中间形成,发生的反应为:2H2+O2 2H2O
2H2O
(1)则负极通的应是H2,负极反应式为 正极反应式为 .
(2)如把KOH改为稀硫酸作导电物质,则负极反应式为 ,
(3)如把H2改为CH4,KOH作导电物质,则负极反应式为 .
(4)写出惰性电极电解以下溶液的总反应的化学方程式
①NaCl溶液
②CuSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
某物质A加热分解,产物都是气体,化学方程式为2A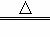 B+2C+2D.测得生成的混合气体对氢气的相对密度为d,则A的相对分子质量为()
B+2C+2D.测得生成的混合气体对氢气的相对密度为d,则A的相对分子质量为()
A. 7d B. 5d C. 2.5d D. 2d
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com