
 .
.分析 根据4s能量小于3d,某元素原子3d轨道上有5个电子,则4s能级上肯定有电子,已知M2+离子3d轨道上有5个电子,则M的原子序数是2+8+13+2=25,即M是Mn元素.
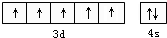
(1)根据构造原理可以得出锰原子的外围电子排布图;
(2)Mn原子的最外层电子数是2个,最高能级是3d,含有5个电子;
(3)锰元素位于元素周期表的第四周期第ⅦB族.
解答 解:(1)M2+离子3d轨道上有5个电子,则M的原子序数是2+8+13+2=25,即M是Mn元素,原子核外有25个电子,所以核外电子排布式为:1s22s22p63s23p63d54s2,其基态原子的外围电子排布式为3d54s2 ,锰原子的外围电子排布图 ,
,
故答案为: ;
;
(2)Mn元素,原子核外有25个电子,核外电子排布式为:1s22s22p63s23p63d54s2,原子的最外层电子数是2个,4s能量小于3d,最高能级是3d,含有5个电子,
故答案为:2;5;
(3)原子核外电子层数与其周期数相等,锰元素位于元素周期表的第四周期,其基态原子的外围电子排布式为3d54s2 ,位于第ⅦB族,
故答案为:第四周期、ⅦB族.
点评 本题考查原子核外电子排布,题目难度中等,把握构造原理是解答关键,侧重考查学生的逻辑推理能力和规范的答题能力.


科目:高中化学 来源: 题型:选择题
 丙泊酚,其化学名为2,6-双异丙基苯酚,是目前临床上普遍用于麻醉诱导、麻醉
丙泊酚,其化学名为2,6-双异丙基苯酚,是目前临床上普遍用于麻醉诱导、麻醉| A. | 分子式为C10H20O | |
| B. | 分子中所有碳原子可能在同一平面中 | |
| C. | 该物质的1H核磁共振谱图中有5个特征峰,峰值强度比大概为:1:1:2:2:12 | |
| D. | 该物质结构中有2个手性碳原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
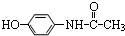 ,则有关它的性质错误的是( )
,则有关它的性质错误的是( )| A. | 与氢氧化钠溶液共热消耗2molNaOH | B. | 能与浓溴水发生取代反应 | ||
| C. | 不能使酸性高锰酸钾溶液褪色 | D. | 遇三氯化铁溶液呈现紫色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列说法不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列说法不正确的是( )| A. | 最高价氧化物对应水化物的酸性:Q<W | |
| B. | 最简单气态氢化物的热稳定性:R>Q | |
| C. | 原子半径:T>Q>R | |
| D. | 含T的盐溶液一定显酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2发生取代反应 | |
| B. | 既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体 | |
| C. | 既可以催化加氢,又可以使酸性KMnO4溶液褪色 | |
| D. | 1 mol该化合物最多可以与3 mol NaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 24Mg32S 晶体中电子总数与中子总数之比为 1:1 | |
| B. | CO2和 PCl5分子中各原子最外层都满足 8 电子结构 | |
| C. | 若 aXm+ 和 bYn- 两种离子电子层结构相同,则 a-b=n-m | |
| D. | 元素周期表中第 4 列元素形成的化合物数目最多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验目的或结论 |
| A | SO2通入溴水中,溶液褪色 | 检验SO2的漂白性 |
| B | 向2mL淀粉溶液中加入稀硫酸,加热2min,加入新制Cu(OH)2在加热,无明显现象. | 淀粉在酸性条件下不水解 |
| C | 将制得的阿司匹林粗产品与饱和碳酸氢钠溶液充分反应后过滤 | 除去阿司匹林中的聚合物 |
| D | 等体积、pH同为3的酸A和B分别与足量的Zn反应,酸A放出的氢气多 | 酸性A比B强 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com