
【题目】下列物质的水溶液能导电,但属于非电解质的是( )
A. CH3COOH B. 蔗糖 C. NH4HCO3 D. CO2
科目:高中化学 来源: 题型:
【题目】一定量的某有机物和足量的钠反应,可得到气体VA L,等质量的该有机物与足量的纯碱溶液反应,可得到气体VB L.若同温、同压下VA>VB , 则该有机物可能是( )
A.HO(CH2)2CHO
B.HO(CH2)2COOH
C.HOOC﹣COOH
D.CH3COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用反应NO2(g)+SO2(g)![]() SO3(g)+NO(g)+Q(Q>0)可处理NO2、SO2等大气污染物,具有十分重要的意义。
SO3(g)+NO(g)+Q(Q>0)可处理NO2、SO2等大气污染物,具有十分重要的意义。
完成下列填空:
(1)该反应中被氧化的元素是__________;写出该反应的平衡常数表达式:K =_____________。
(2)若上述反应在一密闭容器中进行。下列能表明反应达到平衡状态的是_______(选填编号)。
a.混合气体颜色保持不变
b.NO2和NO的体积比保持不变
c.每消耗1mol SO2的同时生成1mol SO3
d.体系中气体密度保持不变
(3)一定温度下,在容积为V L的容器中发生上述反应,t min内,SO2的物质的量下降了a mol,则这段时间内v(NO) =__________(用相关字母表示并注明单位)。
(4)请写出两种能提高SO2转化率的措施:_____________、_____________。
(5)亚硫酸溶液久置,pH会变小,请用方程式表示其原因_______________
(6)将SO2持续通入NaOH溶液中,溶液中SO32—的浓度变化如图所示,请解释原因。
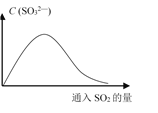
__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去下列物质中的杂质并且不引入新的杂质,所用试剂和方法正确的是( )
选项 | 物质 | 杂质 | 除杂质所用试剂和方法 |
A | CO | CO2 | 通入灼热的CuO |
B | KNO3 | K2SO4 | BaCl2溶液,过滤 |
C | Cu | CuO | 稀硫酸,过滤 |
D | CaCO3 | CaO | 盐酸,过滤 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由乙烯可生产多种化工原料,根据如图所示的转化关系回答问题: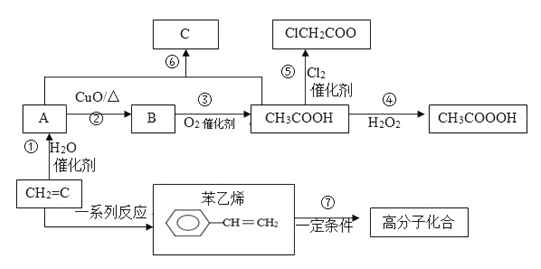
(1)写出下列物质的结构简式:A______;B______;C_______。
(2)反应①~⑦中,属于取代反应的是________(填序号)。
(3)反应②的化学方程式为______________,反应⑦的化学方程式为_________________
(4)苯乙烯是一种重要的化工原料,下列说法正确的___________________
a.该分子中所有原子可能在同一平面上
b.它与足量的H2加成后得到的产物的一溴代物有5种
c.该物质能发生氧化反应和加成反应
(5)重要化工原料氯乙酸(CH2Cl-COOH)与水反应可得到羟基乙酸(HOCH2-COOH),羟基乙酸与反应⑤的产物过氧乙酸互为________(选填“同系物”、“同分异构体”、“同素异形体”或“同位素”);羟基乙酸与乳酸[CH3CH(OH)COOH]的混合物,在浓硫酸作用下脱去一分子水可得到_________种链酯。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一元酸HA溶液中,加入一定量强碱MOH溶液后,恰好完全反应,反应后的溶液中,下列判断一定正确的是( )
A. c(A-)≥c(M+)
B. c(A-)=c(M+)
C. 若MA不水解,则c(OH-)<c(H+)
D. 若MA水解,则c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(N2H4)是一种高能燃料,在工业生产中用途广泛。
(1)肼(N2H4)也可与NO2发生反应,产物均不污染环境。请写出反应方程式:____________________。
(2)肼性质与氨气相似,易溶于水,可发生如下电离过程:
N2H4 + H2O ![]() N2H5+ + OH- I N2H5+ +H2O
N2H5+ + OH- I N2H5+ +H2O ![]() N2H62+ + OH- II
N2H62+ + OH- II
① 常温下,某浓度N2H6Cl2溶液的pH为4,则该溶液中由水电离产生的c(H+)为__________。
② 已知在相同条件下过程I的进行程度大于N2H5+的水解程度。常温下,若0.2 mol/L N2H4溶液与0.1 mol/L HCl溶液等体积混合,则此时溶液呈_________性,溶液中N2H5+、Cl-、OH-、H+、N2H4浓度由大到小的顺序为___________________。

(3)肼和氧气在不同温度和催化剂条件下生成不同产物(如图):
温度较低时主要发生反应a:N2H4(g)+O2(g)![]() N2(g)+2H2O(g)
N2(g)+2H2O(g)
温度较高时主要发生反应b:N2H4(g)+2O2(g)![]() 2NO(g)+2H2O(g)
2NO(g)+2H2O(g)
①若反应b在1000℃时的平衡常数为K1,1100℃时的平衡常数为K2,则K1__________K2。(填“>”、“<”或“=”)
②某温度下,容积固定的密闭容器中,下列描述可说明反应a达到平衡的是_______________。
A.v(N2)=v(N2H4)
B.c(N2H4):c(O2):c(N2)=1:1:1
C.混合气体的密度不再改变
D.体系的压强不再发生变化
E.混合气体的平均相对分子质量不再发生变化
③1000℃,反应b达到平衡时,下列措施能使容器中![]() 变大的是_______。
变大的是_______。
A.恒容条件下充入He B.增大容器体积 C.恒容条件下下充入N2H4 D.使用催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂排放的工业废水中可能含有K+、Ag+、NH4+、Mg2+、SO42-、Cl-、NO3-、HCO3-等离子.经检测废水呈明显的碱性,则可确定该厂废水中肯定不含有的离子组合是
A.Ag+、K+、NO3-、HCO3- B.K+、NH4+、NO3-、SO42-
C.Ag+、NH4+、Mg2+、HCO3- D.K+、Mg2+、SO42-、Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com