
| A. | 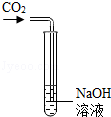 检验生成的气体是CO2 | B. | 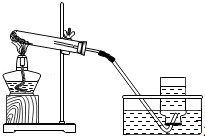 加高锰酸钾制氧气 | ||
| C. | 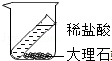 验证质量守恒定律 | D. | 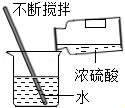 实验室稀释浓硫酸 |
分析 A.二氧化碳通入NaOH溶液中没有明显现象,应该用澄清石灰水检验二氧化碳;
B.加热高锰酸钾制取氧气时,试管内的导气管不能伸入太长;
C.该实验中稀盐酸和大理石生成的二氧化碳无法收集;
D.浓硫酸稀释时应该将浓硫酸沿烧杯内壁倒入水中并不断搅拌.
解答 解:A.二氧化碳通入NaOH溶液中没有明显现象,二氧化碳能使澄清石灰水变浑浊,所以应该用澄清石灰水检验二氧化碳,故A错误;
B.加热高锰酸钾制取氧气时,试管内的导气管不能伸入太长,否则高锰酸钾易堵塞导管,故B错误;
C.该实验中稀盐酸和大理石生成的二氧化碳无法收集,所以无法验证质量守恒定律,故C错误;
D.浓硫酸稀释时应该将浓硫酸沿烧杯内壁倒入水中并不断搅拌,防止局部温度过高而溅出液体,故D正确;
故选D.
点评 本题考查化学实验方案评价,为高频考点,涉及基本实验操作、气体检验等知识点,明确实验原理及基本操作规范性是解本题关键,知道常见气体检验方法,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 原子半径C>A>B>D | B. | 价电子数D>C>A>B | ||
| C. | 离子半径C3+>D->B+>A2+ | D. | 单质的还原性A>B>C>D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
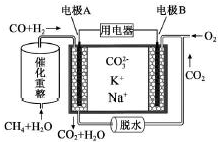
| A. | 正极产物为CO2 | |
| B. | 负极电极反应式为CO-2e-+CO32-═2CO2 | |
| C. | 电池工作时,CO32-向电极A移动 | |
| D. | 电池总反应式为CO+H2+O2═2CO2+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA | |
| B. | 粗铜精炼时,当阳极质量减少6.4 g时,电路中转移的电子数一定不是0.2NA | |
| C. | 含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1NA | |
| D. | 200 mL 0.5 mol•L-1 Na2CO3溶液中,由于CO32-水解,所以阴离子的数目小于0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
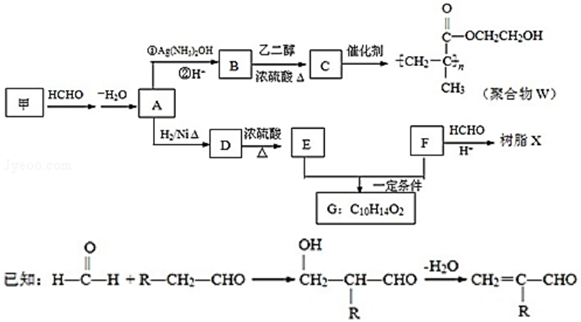
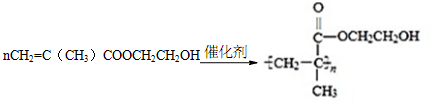 .
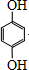
.
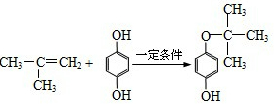 ,反应类型是加成反应.
,反应类型是加成反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 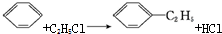 | B. | 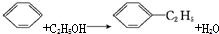 | ||
| C. | 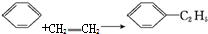 | D. | 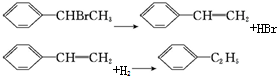 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用小苏打治疗胃酸过多:HCO3-+H+═CO2↑+H2O | |
| B. | Ca(HCO3)2溶液与过量NaOH溶液反应:HCO3-+OH-═CO32-+H2O | |
| C. | 利用腐蚀法制作印刷线路板:Fe3++Cu═Fe2++Cu2+ | |
| D. | 钠与水反应:Na+H2O═Na++OH-+H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com